Lorenzo Romano Amedeo Carlo Avogadro (1776-1856) je bil italijanski kemik, ki je prvi vzpostavil idejo, da vzorec elementa, katerega masa v gramih je numerično enaka njegovi atomski masi, ima vedno enako število atomov (N).
Avogadro sam ni mogel določiti vrednosti N. Vendar pa je skozi dvajseto stoletje napredek tehnologije in znanstvenega znanja omogočal drugim znanstvenikom, da so razvili tehnike za njegovo določitev. Ko so to vrednost končno odkrili, so jo poklicali Avogadrova stalnica, v čast tega znanstvenika, saj je prav on postavil temelje za njegovo ustvarjanje.

Lorenzo Romano Amedeo Carlo Avogadro (1776-1856)
V 1 molu katere koli entitete (atomi, molekule, elektroni, formule ali ioni) je natančno navedena vrednost Avogadrove konstante.
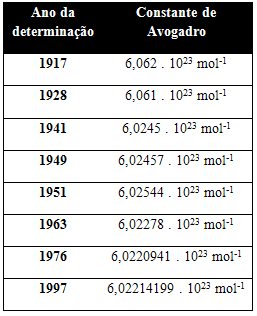
Spodnja tabela prikazuje nekatere vrednosti Avogadrove konstante, pridobljene v 20. stoletju:
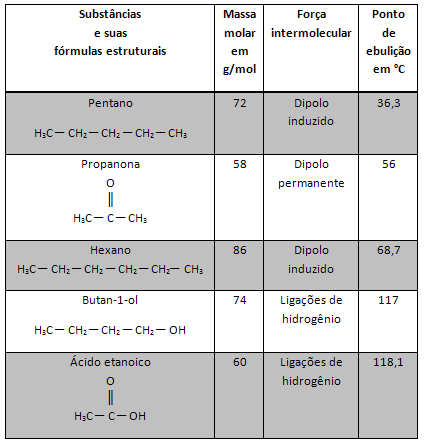
Tu je nekaj tehnik, s katerimi poskušamo določiti vrednost Avogadrove konstante:
Prvi znanstvenik, ki je naredil približen izračun Avogadrove konstante, je bil Johann Joseph Loschmidt. Leta 1867 se je oprl na kinetično teorijo plinov in določil, koliko molekul obstaja v 1 cm
3 plina.Drug od teh znanstvenikov je bil Francoz Jean Baptiste Perrin (1870-1942), ki je v suspenziji prešteval število koloidnih delcev na enoto prostornine in meril njihove mase. Vrednost, ki jo je našel, je bila med 6,5 in 7,2. 1023 entitet na mol. Ta znanstvenik je leta 1913 objavil knjigo Les Atomes (1. izd. Pariz: Alcan) in njegova 9. izdaja, objavljena leta 1924, je vsebovala 16 načinov eksperimentalnega pridobivanja Avogadrove konstante.
Ne ustavi se zdaj... Po oglaševanju je še več;)

Jean Baptiste Perrin (1870-1942)
Leta kasneje je znanstvenik James Dewar (1842-1923) uporabil metodo, ki so jo leta prej razvili radiokemik Bertram Boltwood (1870-1927) in fizik Ernest Rutherford (1871-1937), ki je v osnovi sestavljalo štetje delcev alfa, ki jih oddaja radioaktivni vir, in določanje količine pridobljenega helijevega plina. Vrednost, ki jo je našel Dewar, je bila 6,04. 1023 mol-1.
V 20. stoletju je Robert Millikan (1868-1953) izvedel eksperiment za določitev naboja elektrona (1.6. 10-19 Ç). Ker je bil naboj 1 mola elektronov že znan (96500 C), je bilo mogoče povezati ti dve vrednosti in najti naslednjo vrednost za Avogadrovo konstanto: 6.03. 1023 mol-1.
Trenutno je priporočena vrednost za Avogadrovo konstanto 6,02214 x 1023 mol-1 in se določi z rentgensko difrakcijo, pri kateri dobimo prostornino nekaj atomov kristalne rešetke, če sta znani gostota in masa 1 mola atomov v vzorcu.
Za didaktične namene v srednji šoli, kjer ni treba, da so izračuni natančni kot pri kemijskih laboratorijih, velja Avogadrova konstanta kot 6,02. 1023 mol-1.
Obstajajo tudi enostavnejše metode, s katerimi lahko učenci v praksi ugotovijo Avogadrovo konstanto. Eden od njih je z elektrolizo v vodnem mediju.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Določitev Avogadrove konstante"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/determinacao-constante-avogadro.htm. Dostopno 28. junija 2021.