Katalizatorji so snovi, ki lahko pospešijo reakcijo, ne da bi se spremenile, to pomeni, da se med reakcijo ne porabijo.
Da bi razumeli, kako delujejo katalizatorji, se moramo spomniti, kaj je bilo pojasnjeno v besedilu "Aktivacijska energija”. Kot je prikazano tam, je za začetek kemične reakcije potrebno, da imajo reaktanti določeno količino minimalne energije, ki jo imenujemo aktivacijska energija.
S to minimalno energijo lahko reaktanti dosežejo kompleks aktiviran, ki je vmesno stanje (prehodno stanje), ki nastane med reaktanti in produkti, v katerem strukturi obstajajo oslabljene prejšnje povezave in nastanek novih povezav (prisotnih v izdelkov).
Na primer, razmislite o splošni reakciji spodaj:
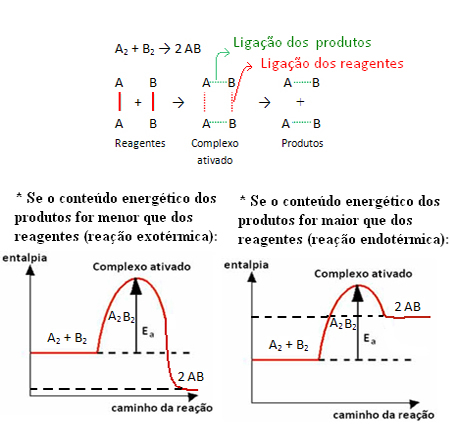
Upoštevajte, da aktivacijska energija, potrebna za doseganje aktiviranega kompleksa, postane neke vrste ovira, ki jo je treba premagati, da se reakcija izvede. To pomeni, da večja kot je aktivacijska energija reakcije, večja je ovira, ki jo je treba premagati, in počasnejša je reakcijska hitrost.
Velja tudi nasprotno, če je aktivacijska energija manjša, bo reakcija hitrejša. Prav to katalizatorji ali jih ustvarijo alternativno pot, ki zahteva manj aktivacijske energije, zaradi česar reakcija poteka hitreje.
Ne ustavi se zdaj... Po oglaševanju je še več;)

Da bi znižal aktivacijsko energijo, katalizator deluje tako, da spremeni reakcijski mehanizem s kombiniranjem z reagenti v sistemu, ki je lahko monofazna (homogena kataliza) ali večfazna (heterogena kataliza).
Več podrobnosti o teh vrstah katalize je razvidno iz spodnjih besedil:
- homogena kataliza
- heterogena kataliza
Toda na splošno lahko rečemo, da to kombinacija reaktanta in katalizatorja tvori vmesno spojino, ki se nato pretvori v produkt in katalizator. Upoštevajte, kako je to mogoče predstaviti:
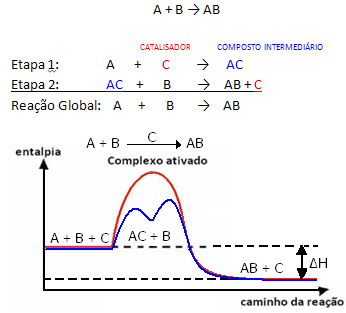
Pazite, da se katalizator ob koncu reakcije regenerira in ga ne porabi.
Pomembno dejstvo je to katalizator pospeši tako naprej kot vzvratno reakcijo, to pomeni, da zmanjša aktivacijsko energijo obeh.
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
FOGAÇA, Jennifer Rocha Vargas. "Kako delujejo katalizatorske snovi?"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/como-atuam-as-substancias-catalisadoras.htm. Dostop 27. junija 2021.