Če bi bilo mogoče zelo jasno predstaviti strukturo kovine, bi jo videli kot na zgornji sliki. Atomska struktura kovin je kristalinična, ki jo sestavljajo kovinski kationi, obdani z elektroni.
Kristalne rešetke v kovinah lahko predstavimo na naslednji način: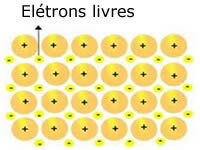
Prikaz kovinskega natrija (Na)
Kristalne rešetke kovin tvori skupina fiksnih kationov.
Vsak Na + kation je obkrožen z elektroni, vendar so ti delokalizirani, torej jih nobeno jedro ne privlači.
Ker med negativnimi naboji (elektron) in pozitivnim jedrom (kation) ni privlačnosti, prosti elektroni na koncu zasedejo celotno kristalno mrežo kovine. Svoboda, po kateri se morajo elektroni premikati, povzroči, da tvorijo elektronski oblak.
Sposobnost kovin za prevajanje električne energije je razložena s prisotnostjo tega oblaka. Električni tok je posledica stika prostih elektronov z drugimi kovinami.
V sestavi katerega koli atoma, vključno s kovinami, kot so natrij (Na), zlato Au, baker (Cu), je valentna plast. Elektroni se prosto gibljejo skozi to plast in ohranjajo elektromagnetno privlačnost kationov. Ta strukturna lastnost omogoča tvorbo kovinskih molekul in posledično samih kovin.
Avtor Líria Alves
Diplomiral iz kemije
Ne ustavi se zdaj... Po oglaševanju je še več;)
Bi se radi sklicevali na to besedilo v šolskem ali akademskem delu? Poglej:
SOUZA, Líria Alves de. "Kako nastane kovinska vez?"; Brazilska šola. Na voljo v: https://brasilescola.uol.com.br/quimica/como-se-forma-ligacao-metalica.htm. Dostopno 28. junija 2021.