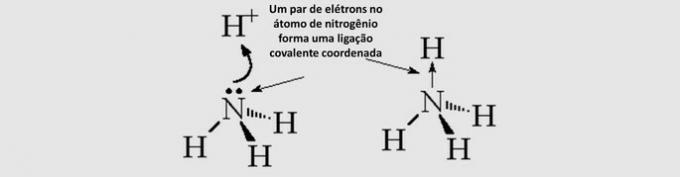
Atomi so neskončno majhni delci, ki tvorijo vso snov v vesolju. Sčasoma se je ideja o tem, kakšna bo atomska struktura, spreminjala glede na nova odkritja znanstvenikov. Več o tem lahko izveste v besediluEvolucija atomskega modela.
Model je predstavitev resničnosti (ne resničnosti same), zato so atomski modeli predstavitve glavne sestavine atoma in njegovo zgradbo ter razloži določena fizikalna in kemijska vedenja snovi. To se naredi, ker človek še z ultramikroskopi še ne more videti izoliranega atoma.
Če želite dobiti idejo, kako majhen je atom, vedite to The Najmanjši delček, viden pod običajnim mikroskopom, vsebuje več kot deset milijard atomov! Atom je tako majhen, da, če bi jih milijon postavili drug ob drugega, ne bi dosegli debelina las.
Zemljevid uma: Atom
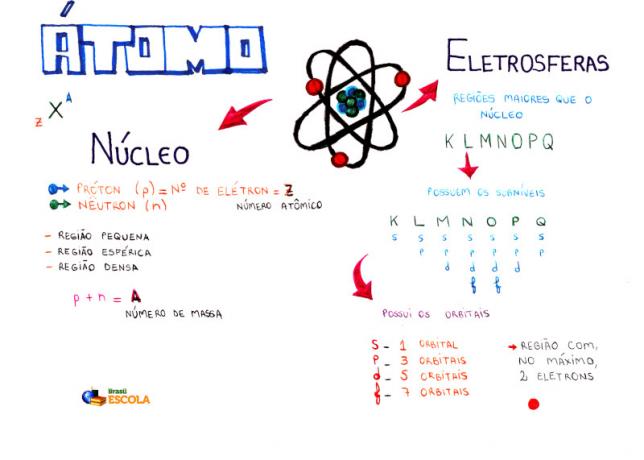
* Če želite prenesti miselni zemljevid v PDF, Klikni tukaj!
Med atomskimi modeli je trenutno v srednji šoli najpogosteje uporabljen Rutherford-Bohrjev model za razumevanje strukture atoma in njegovih lastnosti. V skladu s tem modelom je struktura atoma sestavljena iz dveh glavnih delov: jedro in elektrosfera.

Dva glavna dela zgradbe atoma - elektrosfera in jedro
* Jedro: Kot osrednji del atoma je kompakten, masiven in zelo gost, poleg tega pa ga tvorijo delci z večjo maso, ki so protoni in nevtroni.

Prikaz protonov in nevtronov, ki sestavljajo atomsko jedro
- protoni: so delci s pozitivnim električnim nabojem (relativni naboj = +1; naboj v kulonu (C) = +1,602. 10-19) in njegova relativna masa je enaka 1.
Dejstvo, da protoni tvorijo jedro in mu dajejo splošen pozitiven naboj, je odkril Eugen Goldstein, leta 1886 s spremembo Crookesove ampule in nekaterimi poskusi. Videl je, da se pri zelo visokih napetostih pojavijo emisije (anodni žarki - ostanki atomov plina, ki so bili znotraj žarnice in jim je elektron odtrgal zaradi električnega praznjenja). Z namestitvijo električnega ali magnetnega polja zunaj žarnice so bili ti žarki usmerjeni proti negativnemu polu. To je pomenilo, da obstajajo pozitivni subatomski delci, ki jih imenujemo protoni.
Kasneje, Ernest Rutherford (1871-1937) izvedli poskus, opisan v besedilu Rutherfordov atom, zaradi česar je odkril lokacijo protona: v jedru.
- nevtroni: so delci z maso, enako masi protonov (1), a kot že ime pove, so nevtralni, to pomeni, da nimajo električnega naboja.
Nevtrone je leta 1932 odkril James Chadwick (1891-1974), ki je spoznal, da jedro radioaktivnega berilija oddaja nevtralne delce z maso, približno enako masi protonov (v resnici je nekoliko večja).
Ne ustavi se zdaj... Po oglaševanju je še več;)
Premer jedra je odvisen od količine protonov in nevtronov, ki jih ima atom, v povprečju pa je približno 10-14 mesec in 10-15 m.
Atomsko jedro koncentrira praktično celotno maso atoma, ki je zelo majhen del: tako proton kot nevtron sta približno 100.000 krat manjša od celotnega atoma samega! Za primerjavo si predstavljamo, da povečujemo jedro atoma elementa vodik (ki ima samo protona) do velikosti teniške žogice, najbližji elektron bi bil oddaljen približno tri kilometre razdalja! Tudi če bi atom razširili do višine 14-nadstropne stavbe, bi bilo njegovo jedro velikosti zgolj zrna soli v sedmem nadstropju. Res je nekaj neverjetnega, se vam ne zdi ?!
* Elektrosfera: Je območje, kjer se elektroni vrtijo okoli jedra. Kljub temu da je območje veliko večjega volumna od jedra, je praktično prazno, saj je vsak elektron 1836 krat manjši od 1 protona (ali od 1 nevtrona). Zato je atomska masa praktično vsa v jedru. Elektroni so delci z negativnim električnim nabojem (-1).
Elektrone je leta 1897 odkril Joseph John Thomson (1856-1940), ustvarjalec Thomsonov atomski model. Thomsonov poskus je podrobno razviden iz besedila Thomsonov poskus z električnimi razelektritvami, na kratko pa je uporabil že omenjeno Crookesovo ampulo in spoznal, da so katodni žarki vedno privlačil pozitivni pol, ki je dokazal, da ima atom negativne delce, ki so bili imenovani elektroni.
Elektroni se vrtijo okoli jedra milijarde krat na milijoninko sekunde, oblikujejo atom in se obnašajo, kot da je trden.
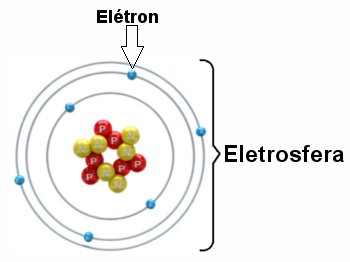
Prikaz elektrosfere s tremi elektronskimi plastmi in elektroni, ki se vrtijo okoli jedra.
Na kratko lahko sestavimo tabelo, v kateri bomo ločili tri glavne subatomske delce, ki so del strukture atoma:

Masa in električni naboj treh glavnih subatomskih delcev - protonov, nevtronov in elektronov
Atomi vseh kemičnih elementov so sestavljeni iz teh treh subatomskih delcev. Kar razlikuje en kemični element od drugega, je količina, v kateri se pojavijo ti delci, zlasti količina protonov v jedru, ki se imenuje atomsko število. Nadaljujte s proučevanjem tega skozi besedilo. Kemični element.
* Mind Map by My Diogo Lopes
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Kemija
Razvrstitev snovi, vode, cianovoda, ogljikov dioksid, amoniak, vodik, helij, snovi enostavne, sestavljene snovi, zmesi, faze zmesi, homogena zmes, zmes heterogena.