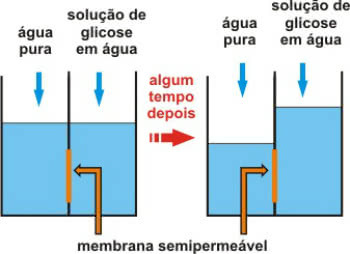
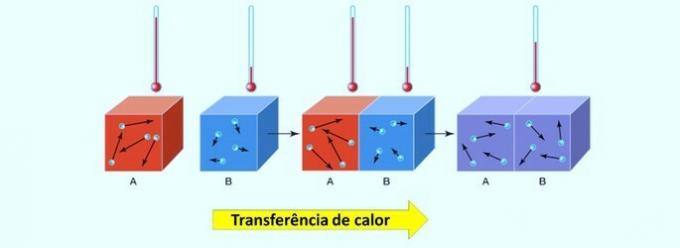
Molekula je niz atomov, enakih ali drugačnih, združenih s kovalentnimi vezmi.
Te kemične vrste so električno nevtralne in predstavljajo tvorbeno enoto snovi.
Obstajajo preproste molekule, kot je kisik (O2) zraka, ki ga dihamo. Obstajajo pa tudi kompleksne spojine, kot npr buckyballs (60 atomov ogljika, vezanih v obliki krogle), ki so največje molekule, ki so jih kdaj našli v vesolju.
Študija molekule
Kovalentna vez v molekuli ustreza delitvi elektronov, običajno med nekovinskimi elementi.
Glej molekulo vode kot primer preproste spojine.
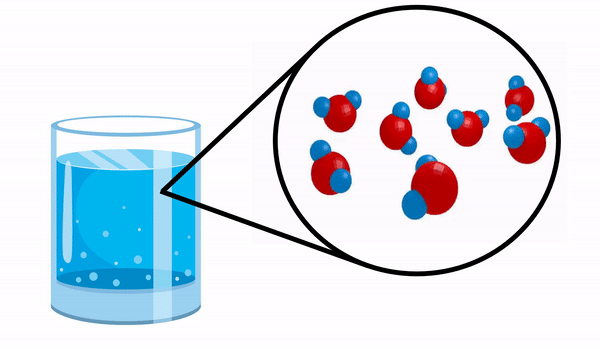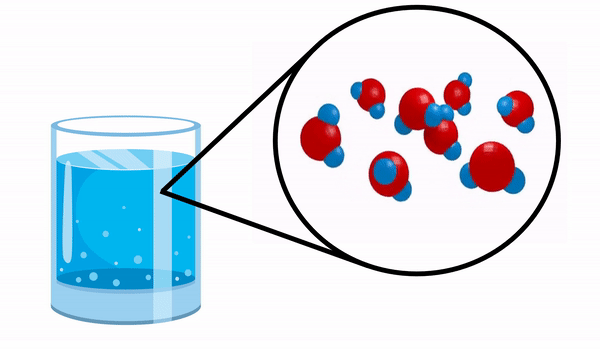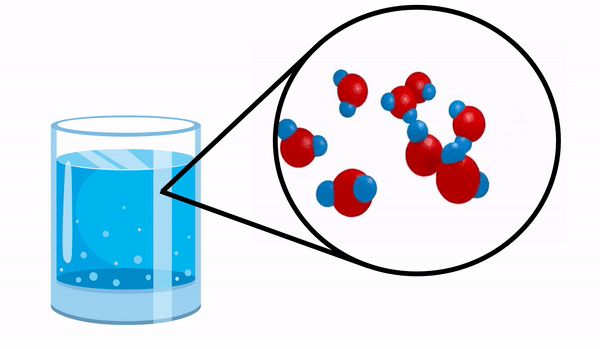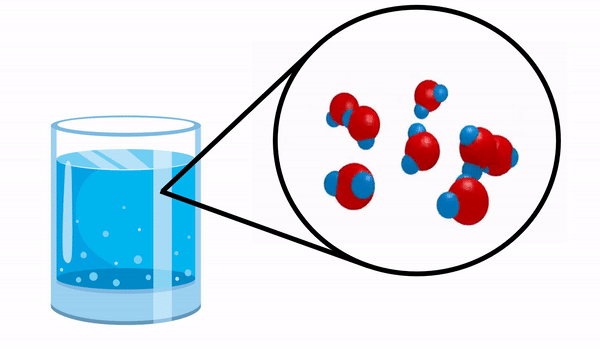
Ko opazujemo kozarec s Voda nimamo pojma, da je ta snov sestavljena iz več molekul H2O. Ta formula kaže, da vodo sestavljajo 3 atomi: dva atoma vodika in en atom kisika, ki si med seboj delijo elektrone.
Sladkor, ki ga uporabljamo za sladkanje sokov in pripravo peciva, je prav tako sestavljen iz molekul. Tvorna enota sladkorja je saharoza.

Ta molekula je veliko bolj zapletena, saj jih je 45 atomi povezan. Sestoji iz: 12 atomov ogljika, 22 atomov vodika in 11 atomov kisika.
Molekule so strukture z znano molekulsko maso, obstajajo pa tudi makromolekule, ki so "velikanske strukture", ki jih tvori toliko atomov, da je njihova sestava celo nedoločena. Primer te vrste je diamant, makromolekula, ki jo tvorijo številni atomi ogljik v kovalentni mreži.
Kovalentna vez
Kovalentna kemijska vez se vzpostavi med dvema atomoma, ko si delita svoja atoma elektroni bolj zunanji (valentni). Molekule imajo lahko dve vrsti vezi:
Molekularna kovalentna vez: par elektronov obeh veznih atomov si delita.

Kovalentna kovalentna vez (dativ): skupni elektroni prihajajo iz samo enega izmed vpletenih atomov.
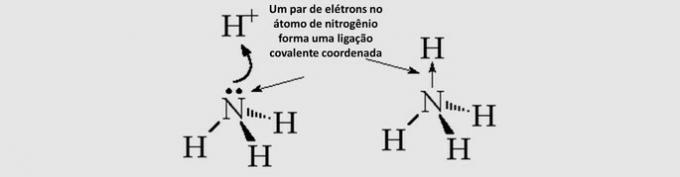
Molekularna geometrija
Ko molekula nastane, so atomi nameščeni na različne načine, tako da je prostorska razporeditev stabilnejša. Zato imajo kompoziti različne geometrije.
Tu je nekaj geometrij, ki jih imajo lahko molekule.
| Molekularna geometrija | ||
|---|---|---|
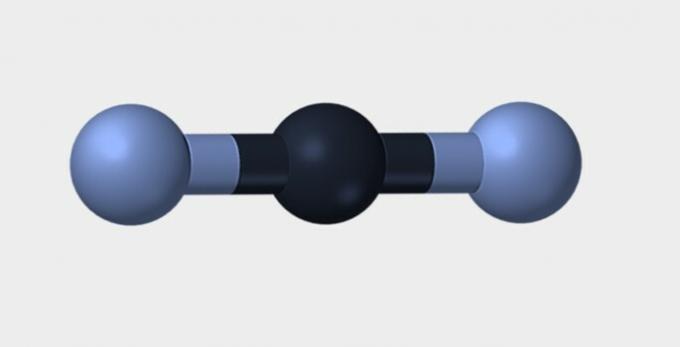
| Linearno | Kotna | Trikotna |
 |
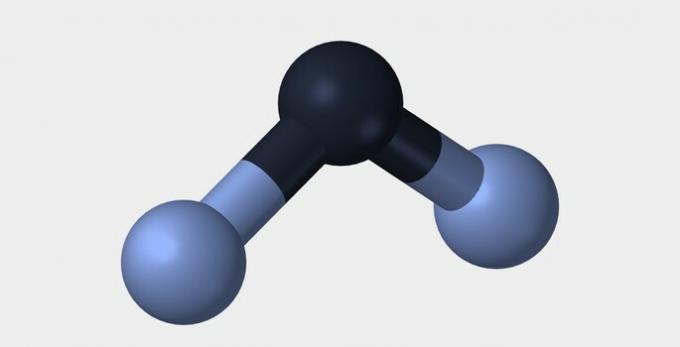 |
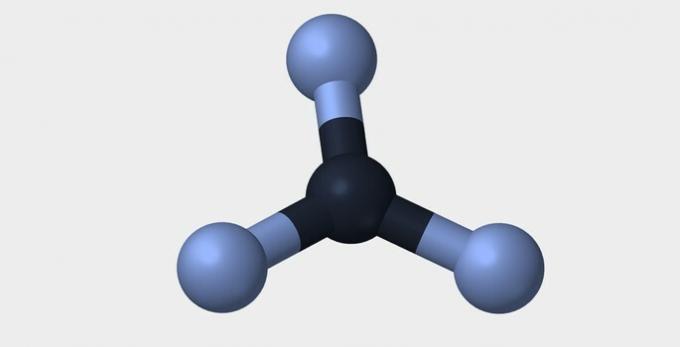 |
| Piramidalni | tetraedrski | oktaedrski |
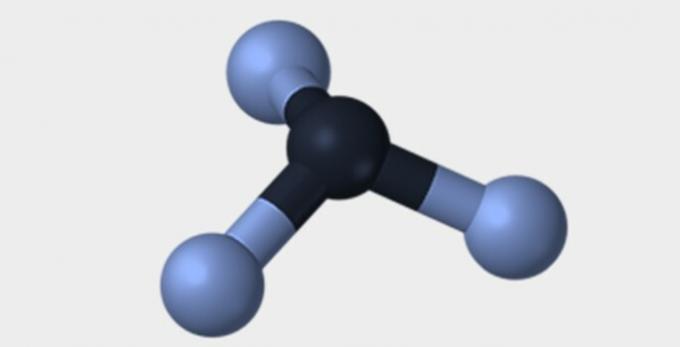 |
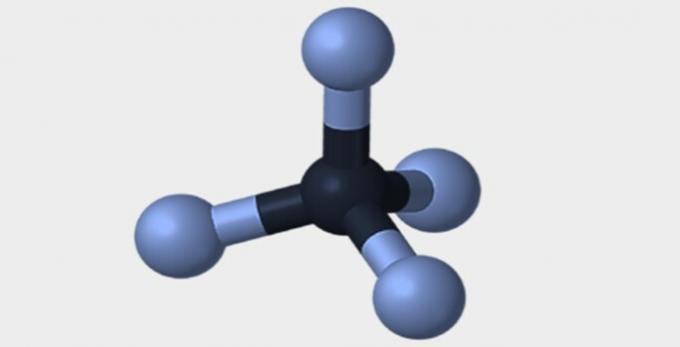 |
 |
Polarne in nepolarne molekule
Molekule so razvrščene glede na polarnost.
nepolarne molekule: med atomi ni razlike v elektronegativnosti.
| Dušik (N2) | ogljikov dioksid (CO2) |
|---|---|
 |
 |
Dušik (N2) je nepolarna molekula, ker jo tvori. kemični element in zato ni razlike v elektronegativnosti. ogljikov dioksid (CO2) je nepolaren zaradi svoje linearne geometrije, ki stabilizira privlačnost kisika z elektroni.
polarne molekule: razlika med elektronegativnostjo med atomi je pozitivna in negativna.
| Voda (H2O) | Amoniak (NH3) |
|---|---|
 |
 |
V obeh primerih vidimo, da imajo osrednji atomi, kisik in dušik, neparne elektronske pare, ki tvorijo elektronske oblake. Ker je okoli osrednjih atomov več elektronskih oblakov, kot je vzpostavljenih kemičnih vezi, so molekule polarne.
Primeri molekul
| Snov | Lastnosti | Molekula | Formula |
|---|---|---|---|
| Vodik | Goriva in veliko v zemeljski skorji. | 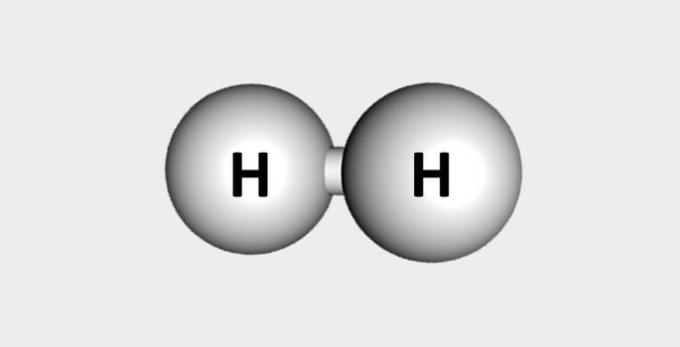 |
H2 |
| Kisik | Bistven za dihanje in sodeluje v različnih kemijskih reakcijah | 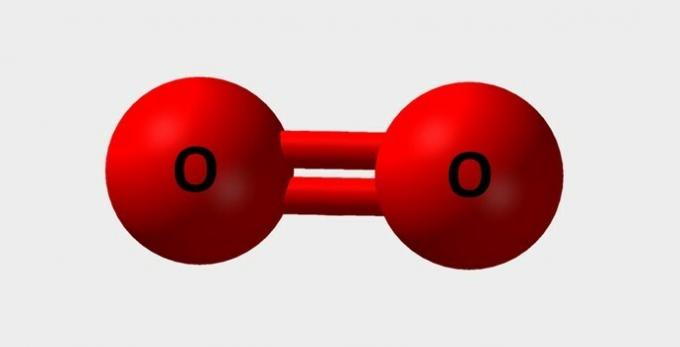 |
O2 |
| Žveplo | Rumeni prah, ki se uporablja za izdelavo barvil. | 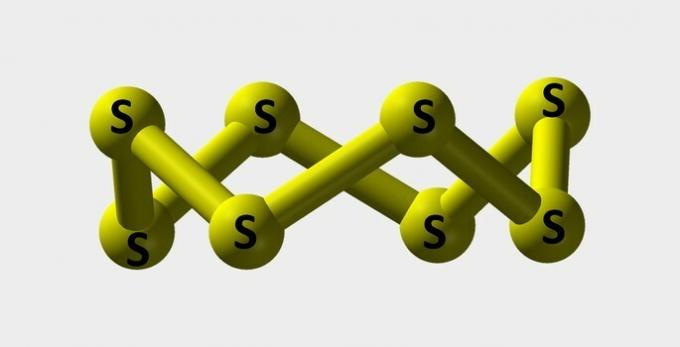 |
s8 |
| Ogljikov dioksid | Uporablja se v gasilnih aparatih in hladilnih sredstvih. | 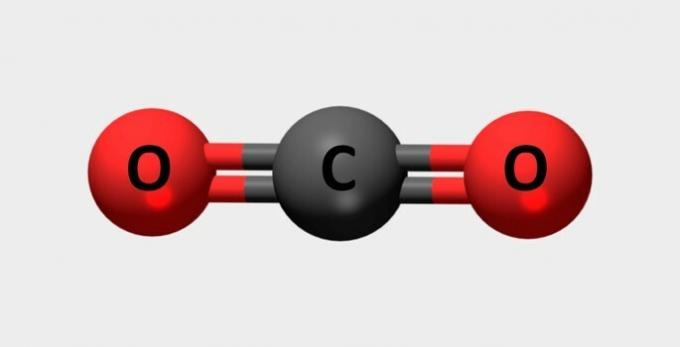 |
CO2 |
| Etanol | Običajni alkohol, ki se uporablja kot gorivo in v parfumih. | 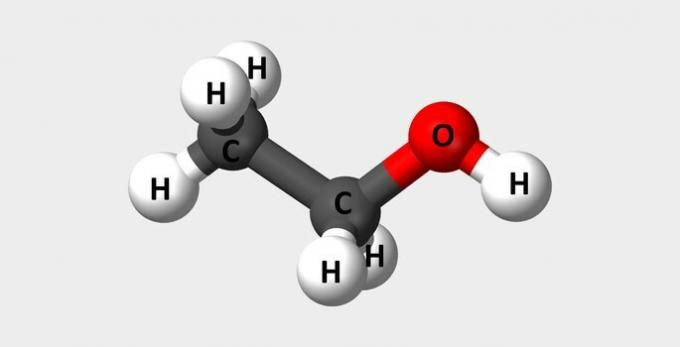 |
Ç2H6O |
Preverite ta besedila o temah, povezanih s tem, kar ste se pravkar naučili:
- Biomolekule
- Organske spojine
- Molekulska masa
- Pravilo okteta
- Kemične vezi
- Polarnost povezave
- Medmolekularne sile