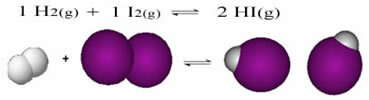
Chemickou rovnicou sa rozumie opis chemických procesov, v ktorých sú zobrazené reaktanty a produkty zúčastňujúce sa na reakcii:
C + O2→ CO2
Činidlá produktu
Aby došlo k chemickej väzbe, musí dôjsť k prerušeniu existujúcich väzieb v reaktantoch a k vytvoreniu nových väzieb v produktoch. Tento proces zahŕňa štúdium energetických variácií reakcií.
Dodávka energie umožňuje prerušenie väzby reaktantov (endotermický proces), zatiaľ čo tvorba väzieb v produkte je exotermický proces, pretože sa uvoľňuje energia.
Väzbová energia je tá, ktorá sa uvoľňuje pri tvorbe produktu a je číselne rovnaká ako energia absorbovaná pri pretrhnutí tejto väzby, takže väzobná energia je definovaná pre prerušenie väzieb.
Stručne zhrnuté: Energia väzby je energia absorbovaná pri lámaní 1 molu väzieb v plynnom stave pri 25 ° C a 1 atm.
Teraz si pozrite príklad, ako získať väzbovú energiu reakcií:
HCl (g) → H (g) + Cl (g) ∆H = + 103,0 Kcal / mol
Teraz neprestávajte... Po reklame je toho viac;)
Vyššie uvedená rovnica ukazuje, že rozbiť väzby na 1 mol molekúl HCl (g) a vytvoriť 1 mol atómov HCl H (g) a 1 mol atómov Cl (g) sú potrebné, 103,0 kcal, tj väzbová energia HCl (g) = + 103,0 Kcal / mol.
Stabilita väzby: čím vyššia je energia väzby, tým je väzba stabilnejšia. Príklad:
Ak sú dané nasledujúce väzbové energie:
H2O (1) → H2 (g) + O (g) ∆H = + 110,6 Kcal / mol
HBr (g) → H (g) + Br (g) ∆H = + 88,0 Kcal / mol
Aká by bola najstabilnejšia väzba, ktorá je prítomná v HBr alebo H2O?
Energia viažuca vodu (H2O) má vyššiu hodnotu ako HBr, takže má väčšiu stabilitu.
Líria Alves
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
SOUZA, Líria Alves de. „Väzbová energia v chemických rovniciach“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/energia-ligacao-equacoes-quimicas.htm. Prístup k 28. júnu 2021.