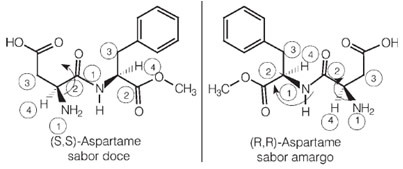
O organické adičné reakcie sú veľmi časté a študované. Je potrebné pripomenúť, že ide o typ reakcie, ktorá predstavuje základný a prevažujúci mechanizmus rozbiť odkaz, alebo odkazy, pi takže dva alebo viac atómov môže začať byť súčasťou reťazca.
Príklad použitia adičných reakcií súvisí s výroba margarínu. Tento produkt, tak bežný v každodennom živote ľudí, vzniká hydrogenáciou (adičnou reakciou) prítomných rastlinných olejov pí odkazy vo svojej ústave.
Typy adičných reakcií sú:
hydrogenácia (pridanie atómov vodíka);
Halogenácia (prídavok atómov halogénu: Cl2, br2, Ja2 a F2);
Reakcia s halogenidom (pridanie anorganických hydrokarbov obsahujúcich halogén, ako je HCl, HI, Hbr a HF);
Hydratácia (prídavok hydrónia, H+a hydroxylovú skupinu, OH-).
Počas pridávania o hydratácia alebo halogenid, The Vláda Markovnikova je pre nás kľúčové predpovedať produkty, ktoré sa budú vyrábať. V tomto pravidle máme tento atóm hydrónium (H+) z anorganického hydroxidu alebo vody sa pridá do viac hydrogenovaného uhlíka
dvojitej väzby. už je halogén (Cl, Br, I, F) halogenidu alebo hydroxyl (OH-) vody sa pridá do menej hydrogenovaného uhlíka odkazu pí. Príklad uplatnenia tohto pravidla nájdete v nasledujúcej rovnici: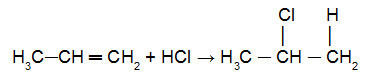
Reakcia proprénu s HCl
Na tejto rovnici vidíme, že atóm o (Cl) bol pridaný k menej hydrogenovanému uhlíku z pí odkaz, zatiaľ čo atóm hydrónium (H+) sa pridal k najviac hydrogenovanému atómu uhlíka z pí odkaz.
je tu iba jeden výnimkou k pravidlu Markovnikova: Kharashova reakcia. V ňom dôjde k inverzii, to znamená k atómu hydrónium (H+) bude pridaný do menej hydrogenovaného uhlíka dáva pí odkaz, to je halogén (Br) halogenidu sa pridá k viac hydrogenovaného uhlíka dáva pí odkaz. Podrobnosti sú také, že táto reakcia sa vyskytuje iba jedným spôsobom:
Teraz neprestávajte... Po reklame je toho viac;)
Prítomnosť organického peroxidu;
Použitie Hbr.
POZNÁMKA: ak nie sú splnené tieto podmienky, Vláda Markovnikova sa bude bežne používať.
Nižšie je uvedená aplikácia Kharashova reakcia v propyléne:
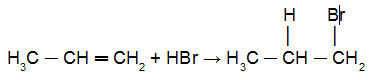
Reakcia propénu s HBr v prítomnosti peroxidu
POZNÁMKA: Je potrebné poznamenať, že organický peroxid je zlúčenina, ktorá nevyhnutne obsahuje skupinu (R─O─O─R). Najpoužívanejší organický peroxid pri Kharashových reakciách je odvodený od karboxylových kyselín a má nasledujúcu štruktúru:
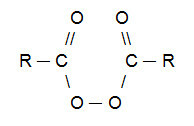
Všeobecný štruktúrny vzorec organického peroxidu
Vysvetlenie Kharashovej reakcie na zvrátenie pravidla Markovnikova spočíva v skutočnosti, že spočiatku sa rozkladá peroxid (krok 1), ktoré tvoria voľné radikály s dvoma atómami kyslíka, ktoré napádajú vodík HBr (Krok 2). Z tohto dôvodu bude na začiatku útočiť na molekulu alkénu Br (krok 3). Až potom, keď sa vodík naviaže na alkénový reťazec. Postupujte podľa sledu faktov:
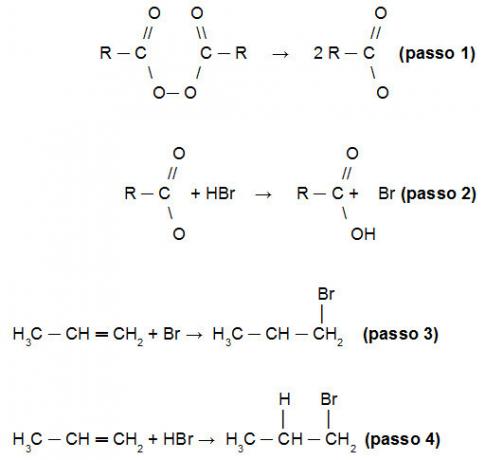
Ukážka mechanizmu Kharashovej reakcie
Podľa mňa. Diogo Lopes Dias
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
DNI, Diogo Lopes. „Kharashova reakcia“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/reacao-kharash.htm. Prístup k 28. júnu 2021.