Adičné reakcie sú tie, pri ktorých sa reaktant pridáva k organickej molekule.
Vyskytujú sa hlavne v nenasýtených zlúčeninách, najmä alkénoch, a vyskytujú sa, ako je znázornené všeobecne nižšie, kde je dvojitá alebo trojitá väzba prerušená. V skutočnosti odkaz pi (π), ktorý je slabší ako sigma odkaz (σ) z dvojitej látky je prerušený, čo umožňuje pridanie atómov alebo skupín atómov k uhlíkom, ktoré sa podieľali na nenasýtení.
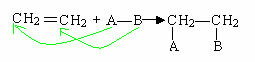
Najbežnejšie adičné reakcie sú:
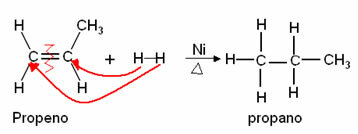
1. Pridanie vodíka (Hydrogenácia alebo Sabatier-Senderensova reakcia): Reakcia s plynným vodíkom (H2), katalyzované kovom. Ak je reakciou alkén, produkuje alkán:
2. Pridanie halogénov (Halogenácia): Halogény sú prvkami rodiny 17A periodickej tabuľky. Z nich sa však najviac používajú: Cl2 a br2. V tomto prípade dôjde k vytvoreniu alkylového dialektu:
Teraz neprestávajte... Po reklame je toho viac;)

3. Pridanie halogénhydridov (Hydrohalogenácia): Halogenid (HX) je zlúčenina, v ktorej je halogén viazaný na vodík, napr. Chlorovodík z nasledujúcej reakcie, za tvorby alkylhalogenidu:
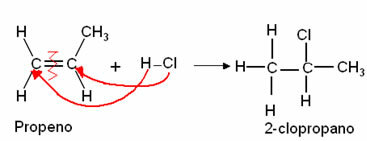
Je dôležité mať na pamäti, že táto a ďalšia reakcia sa riadi Markovnikovovou regiochémiou, pri ktorej vodík vstupuje do najviac hydrogenovaného uhlíka. *
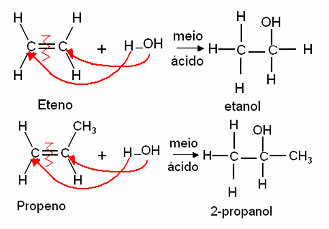
4. pridanie vody: Táto hydratačná reakcia prebieha v kyslom prostredí ako katalyzátor a vytvára sa alkohol. S výnimkou etylénu zvyšujú ostatné alkény v tejto reakcii iba sekundárne alkoholy:
* Podrobnejšie vysvetlenie regiochémie Markovnikov nájdete v texte „Markovnikovovo pravidlo” .
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Dodatočné reakcie“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/reacoes-adicao.htm. Prístup k 27. júnu 2021.