THE periodická klasifikácia prvkov navrhol v roku 1913 Henry Monseley (1887-1915), ktorý identifikoval periodické variácie mnohých vlastnosti v pravidelných intervaloch podľa počtu protónov v jadre atómu prvku chemický.
Kvôli Zákon periodicity, kritérium používané na usporiadanie prvkov súčasnej periodickej tabuľky je vzostupné poradie atómového čísla (Z).
118 chemických prvkov je usporiadaných do skupín a období periodickej tabuľky. Podľa fyzikálnych a chemických vlastností je možné rozlišovať medzi kovy, nekovy (nekovy) a polokovy (metaloidy).

Zvislé čiary sú 18 skupín tabuľky a spájajú prvky s podobnými chemickými vlastnosťami. Vodorovné čiary zodpovedajú 7 období a predstavuje prvky s rovnakým počtom elektronických vrstiev.
Vodík je prvok, ktorý sa nachádza nad skupinou 1 kvôli jeho elektronickej distribúcii, ale nemá s nimi spoločné vlastnosti.
Pozrite sa na Periodická tabuľka kompletné a aktualizované.
kovy
Väčšina chemických prvkov v periodickej tabuľke je klasifikovaná ako kovy. Hlavné vlastnosti kovov sú:
- Majú charakteristický lesk;
- Sú husté, kujné a tvárne;
- Sú dobrými vodičmi elektriny a tepla;
- V podmienkach okolia sú prítomné v pevnom stave, s výnimkou ortuti.
Kovové prvky periodickej tabuľky sú:
alkalických kovov (skupina 1): lítium, sodík, draslík, rubídium, cézium a francium.
kovy alkalických zemín (skupina 2): berýlium, horčík, vápnik, stroncium, bárium a rádium.
Reprezentatívne záležitosti, okrem prvkov skupiny 1 a 2, sú to: hliník, gálium, indium, tálium, nion, cín, olovo, flerovium, bizmut, muscovium a livermorium.
Vonkajšie prechodné kovy sú prvky, ktoré zaberajú centrálnu časť periodickej tabuľky:
- Skupina 3: skandium a ytrium.
- Skupina 4: titán, zirkónium, hafnium a rutherfordium.
- Skupina 5: vanád, niób, tantal a dubnium.
- Skupina 6: chróm, molybdén, volfrám a seborgium.
- Skupina 7: mangán, technécium, rénium a bohrium.
- Skupina 8: železo, ruténium, osmium a hassium.
- Skupina 9: kobalt, ródium, irídium a meitnérium.
- Skupina 10: nikel, paládium, platina, darmštadium.
- Skupina 11: meď, striebro, zlato a röntgen.
- Skupina 12: zinok, kadmium, ortuť a kopernicium.
Vnútorné prechodné kovy sú prvky, ktoré sú súčasťou skupiny 3 a zodpovedajú prvkom radu lantanoidov a aktinidov.
Séria lantanoidov pozostáva z lantánu, céru, prazeodýmu, neodýmu, prométia, samária, európia, gadolínia, terbia, dysprózia, holmia, erbia, thúlia, ytterbia a lutécia.
Aktinidový rad obsahuje prvky aktínium, tórium, protaktínium, urán, neptunium, plutónium, amerícium, kúrium, berkelium, kalifornium, einsteinium, fermium, mendelevium, nobelium a laurencia.
Prečítajte si viac o alkalických kovov.
nekovy
Nekovy sa nachádzajú v pravej časti periodickej tabuľky a majú opačné vlastnosti ako kovy, napríklad:
- Nemajú lesklý vzhľad;
- Nie sú dobrými vodičmi elektriny a tepla, preto sa používajú ako izolanty;
- Majú nízke teploty varu a topenia, takže mnohé sa v prírode nachádzajú v tekutom stave.
vy nekovové prvky periodickej tabuľky sú: vodík, dusík, kyslík, uhlík, fosfor, selén, síra, halogény a vzácne plyny.
vy halogény sú prvky, ktoré patria do skupiny 17: fluór, chlór, bróm, jód, astatín, tenessín a rodina vzácnych plynov.
vy vzácnych plynov sú prvky, ktoré patria do skupiny 18: hélium, neón, argón, kryptón, xenón, radón, oganezón.
Zistite viac o vzácnych plynov a halogény.
polokovy
Polokovy alebo metaloidy sú: bór, kremík, germánium, arzén, antimón, telúr a polónium. Tieto prvky majú vlastnosti, ktoré sú medzi kovmi a nekovmi.
Prečítajte si tiež o rodiny periodickej tabuľky.
Reprezentatívne a prechodové prvky
Ďalším spôsobom klasifikácie prvkov je ich rozdelenie na reprezentatívne a prechodové prvky podľa elektronické rozloženie atómu.
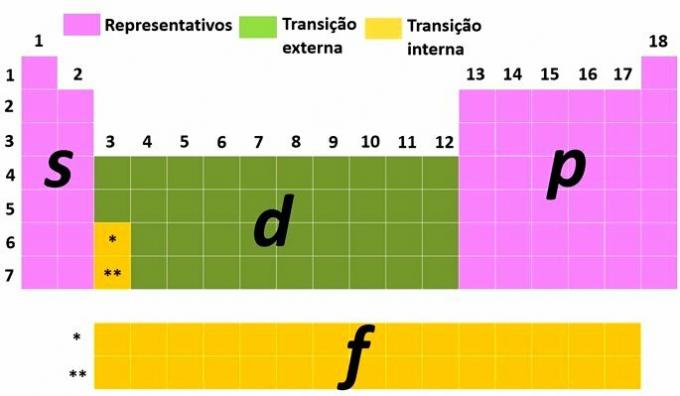
vy reprezentatívne prvky sú tie, ktoré majú elektronickú konfiguráciu končiacu najenergickejšou podúrovňou v s (skupina 1 a 2) príp pre (skupiny 13, 14, 15, 16, 17 a 18).

vy prechodové prvky sú rozdelené do vonkajší prechod, s prvkami, ktoré majú najenergetickejší elektrón v podúrovni d a tie z vnútorný prechod, kde najenergetickejší elektrón je v podúrovni f.

Získajte viac vedomostí s obsahom:
- periodické vlastnosti
- Cvičenia s periodickou tabuľkou
- Cvičenia o organizácii periodickej tabuľky

