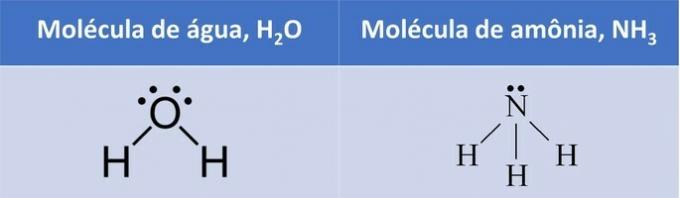
THE izoméria je to jav pozorovaný, keď sú rôzne zlúčeniny tvorené rovnakými množstvami rovnakých typov atómov.
Preto môžeme nájsť chemické látky s rovnakým molekulovým vzorcom a odlišným štruktúrnym vzorcom alebo priestorovým usporiadaním.
Tento jav je široko pozorovaný v organickej chémii, ktorá študuje zlúčeniny uhlíka. Keďže každý atóm tohto prvku môže vytvárať 4 chemické väzby, je možné pozorovať rôzne kombinácie.
Keďže zmena v usporiadaní atómov vedie k vzniku nových látok, majú v dôsledku toho rôzne fyzikálne a chemické vlastnosti.
Keď povieme, ktoré zlúčeniny sú izoméry znamená, že majú rovnaké časti, keďže slovo je kombináciou dvoch výrazov gréckeho pôvodu: isos, znamená „naozaj“ a obyčajné, čo sú „časti“.
Dve hlavné skupiny izomérie sú rovina a priestor (stereoizoméria).
THE plochá izoméria dá sa vizualizovať plochým štruktúrnym vzorcom zlúčenín a má päť tried: poloha, funkcia, reťazec, kompenzácia a tautoméria.
THE priestorová izoméria pozoruje sa orientáciou zlúčenín a delí sa na geometrické (cis-trans) a optické.
Pojem izoméria zaviedol v roku 1830 švédsky vedec Jacob Berzelius.
Príklady izomérov
THE reťazová izoméria vyskytuje sa, keď sa rovnaký súbor atómov spája a vytvára štruktúry rovnakej funkčnej skupiny, ale s rôznymi reťazcami.
Príklad: molekulový vzorec C4H10 uhľovodíka môže byť priamy alebo rozvetvený.

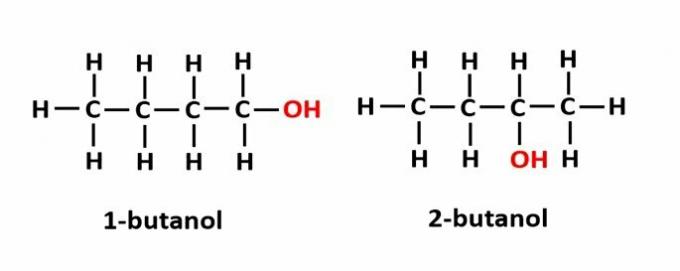
THE polohová izoméria nastáva, keď sú zlúčeniny tvorené rovnakými funkčnými skupinami, ale sú na rôznych pozíciách v reťazci.
Príklad: Molekulový vzorec C4H9OH zodpovedá dvom druhom alkoholu.
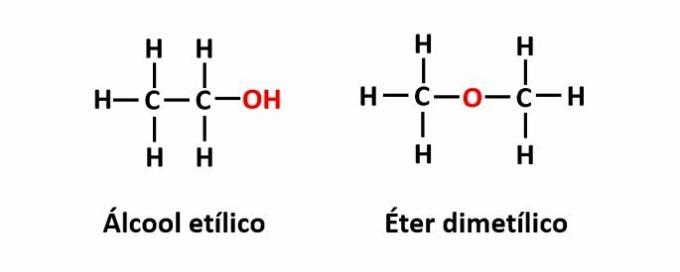
THE izoméria funkcie nastáva, keď rovnaký molekulový vzorec zodpovedá dvom zlúčeninám s rôznymi funkčnými skupinami.
Príklad: Molekulový vzorec C2H6O zodpovedá dvom izomérom, ktoré majú alkoholovú (-OH) a éterovú (-O-) funkciu.
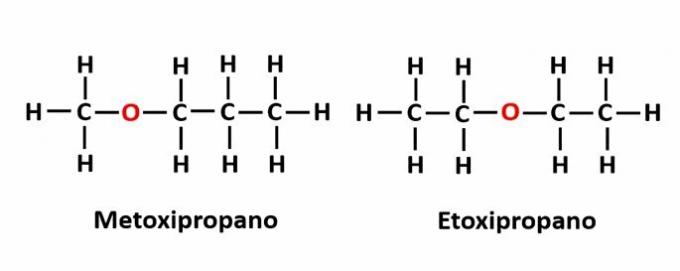
THE kompenzačná izoméria vyskytuje sa, keď je v reťazci heteroatóm a ten obsadzuje rôzne pozície. Toto je zvláštny prípad pozičnej izomérie.
Príklad: Molekulový vzorec C4H10Symbol označuje prítomnosť atómu kyslíka v reťazci, ale jeho poloha sa môže meniť a vytvárať rôzne zlúčeniny.
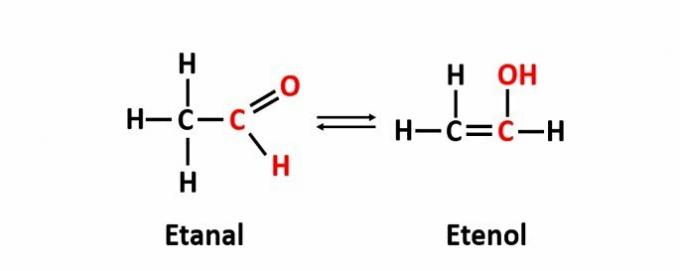
THE dynamická izoméria, tiež nazývaná tautoméria, nastáva, keď sú dve zlúčeniny s rôznymi funkciami v rovnakom roztoku v dynamickej rovnováhe. Toto je špecifický prípad funkčnej izomérie.
Príklad: Molekulový vzorec C2H4O zodpovedá zlúčeninám s aldehydovými a enolovými funkciami.
Naučiť sa viac o plochá izoméria.
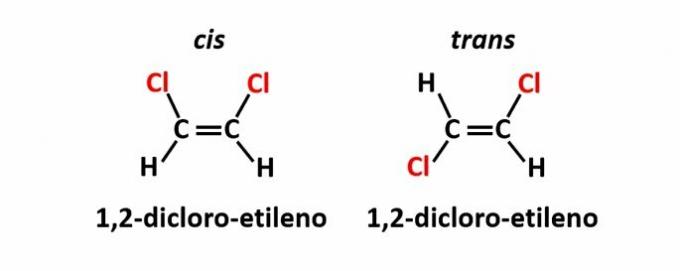
THE geometrická izoméria, tiež nazývaný izoméria cis-trans, nastáva, keď prítomnosť dvojitej väzby alebo cyklickej štruktúry spôsobí, že rovnaké ligandy sú na rovnakej strane roviny (cis) alebo na opačných stranách (trans).
Príklad: atómy chlóru v zlúčeninách molekulového vzorca C2H2Cl2 môžu mať dve priestorové štruktúry.
THE optická izoméria nastáva, keď pri vychyľovaní polarizovaného svetla vyžarovaného na štruktúru zlúčeniny dokážu vychýliť lúč svietiace vľavo, ak ide o ľavotočivý (l) izomér, alebo vpravo, ak ide o pravotočivý izomér (d).
Príklad: Tento typ izomérie sa vyskytuje pri kyseline mliečnej. Všimnite si nižšie, že spektrálne obrazy izomérov sa neprekrývajú, preto sa nazývajú enantioméry.
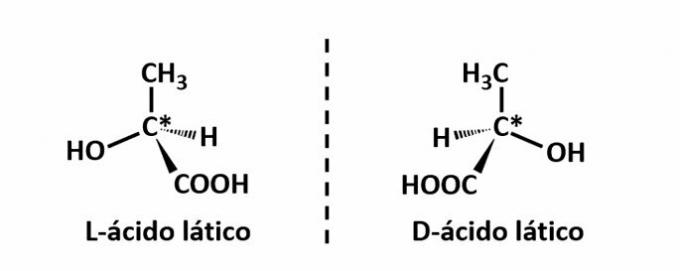
Symbol C* označuje prítomnosť chirálneho uhlíka v tejto štruktúre, tj atóm uhlíka so 4 rôznymi linkermi.
Prečítajte si viac o izomérii s obsahom:
- Typy izomérie
- priestorový izomér
- geometrický izomér
- optický izomér
- Cvičenia o rovinnej izomérii