- Neutrálne médium:
Médium sa považuje za neutrálne, ak má rovnakú koncentráciu hydróniových iónov v mol/l (H3O+) a hydroxid (OH-).
Príkladom neutrálneho média, ktoré dokonca slúži ako štandard pre iné roztoky, je čistá destilovaná voda s teplotou 25ºC. Pri tejto teplote má presne 1. 10-7 mol/l oboch iónov. Preto váš iónový produkt (Kw) sa rovná 10-14 (mol/l)2:
Kw = [H3O+]. [och-]
Kw = (1. 10-7 mol/l). (1. 10-7 mol/l) = 10-14 (mol/l)2
Hodnoty pH a pOH sú uvedené nižšie:
pH= - log [H3O+pOH= -log[OH-]
pH= - log 1. 10-7 pOH= - log 1. 10-7
pH = 7pOH = 7
To nám ukazuje, že v neutrálnom riešení je pH sa rovná pOH.
- Kyslé médium:
V kyslom prostredí je koncentrácia H iónov3O+ je väčšia ako u OH iónov-.
Takéto riešenie je možné dosiahnuť pridaním malej časti H iónov3O+napríklad pomocou kyseliny.
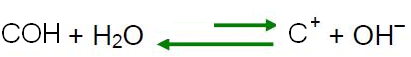
Podľa Le Chatelierovho princípu, keď je v rovnovážnom systéme spôsobená porucha, má tendenciu sa sám prestavovať, aby sa znížili účinky tejto sily. To znamená, že ak sa do vody pridá kyselina, H ióny3O+ budú v prebytku a rovnováha sa posunie v opačnom smere reakcie, doľava. Takže tieto prebytočné ióny budú reagovať s OH iónmi
-. Teda koncentrácia OH iónov- sa zníži a roztok sa stane kyslým.Neprestávaj teraz... Po reklame viac ;)

Iónový produkt (Kw) sa vždy rovná 10-14, ale koncentrácia H iónov3O+ je väčšia ako koncentrácia OH iónov-1. Preto je pH vyššie ako pOH v kyslom prostredí, ale jeho súčet sa vždy rovná 14.
Tiež, čím väčšia je koncentrácia H iónov3O+tým väčšia je hodnota pH. Pri teplote miestnosti (25 °C), pH < 7 a pOH > 7.

- Základné prostriedky:
V základnom prostredí koncentrácia OH iónov- je väčšia ako u H iónov3O+.
Ak do vody pridáme zásadu, znamená to, že pridávame OH ióny.- a, ako je vysvetlené v predchádzajúcom bode, podľa Le Chatelierovho princípu, rovnováha reakcie samoionizácia vody sa bude pohybovať opačným smerom, pričom nadbytočné ióny budú reagovať s H ióny3O+, znížte svoju koncentráciu a urobte roztok zásaditým.
V takom prípade bude pOH vyššie ako pH. Pri teplote miestnosti (25 °C), pH > 7 a pOH < 7.

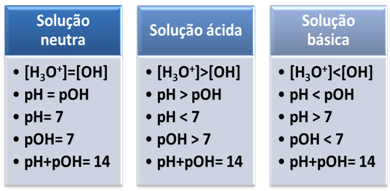
Stručne:
Autor: Jennifer Fogaça
Vyštudoval chémiu
Chceli by ste odkázať na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. "Neutrálne, kyslé a zásadité médiá"; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/meios-neutro-acido-basico.htm. Prístupné 27. júla 2021.

