reakcie s zásadité oxidy sú chemické javy, pri ktorých je látka tejto triedy oxidov umiestnená v tej istej nádobe ako a anorganická kyselina, a kyslý oxid alebo jeden amfotérny oxid.
Pozri tiež:Reakcie s amfotérnymi oxidmi
anorganická soľ a voda sú bežné produkty v a reakcia so zásaditými oxidmi. Aby sme zistili, či sa bude vyrábať anorganická soľ alebo voda, musíme sa pozrieť na látku, ktorá sprevádza zásaditý oxid v činidle. Pozrite si príklady nižšie a pochopte, ako tento proces prebieha.
Reakcie so zásaditými oxidmi a anorganickými kyselinami
Pri reakciách medzi zásaditými oxidmi a anorganickými kyselinami vzniká anorganická soľ a voda, pretože zásaditý oxidový katión (Y+) interaguje s aniónom (X-) kyseliny a hydroniový katión (H+) kyseliny interaguje s aniónom oxidu:
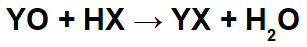
Príklad: Oxid raditý a kyselina bromovodíková
V tejto reakcii máme ako reaktanty oxid rádium (RaO) a kyselinu bromovodíkovú (Hbr). Dochádza teda k nasledujúcim interakciám:
Rádiový katión (Ra+2) s bromidovým aniónom (Br-1) za vzniku soli bromidu rádia (RaBr2).
Hydroniový katión (H+1) s oxidovým aniónom (O-2) tvoriaca vodu (H2O).
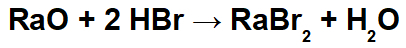
Pozri tiež:Reakcie s dvojitými oxidmi
Reakcie so zásaditými oxidmi a kyslými oxidmi
Pri týchto reakciách vzniká anorganická soľ prostredníctvom interakcie medzi zásaditým oxidovým katiónom (Y+) a výsledný kyslý anión (WOThe-) chemickej reakcie medzi kyslým oxidom a vodou.
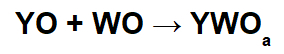
Príklad: Oxid sodný a oxid siričitý
V tejto reakcii máme oxid sodný (Na2O) a oxid siričitý (SO2). Je pozoruhodné, že spočiatku, keď kyslý oxid interaguje s vodou, dochádza k tvorbe kyseliny sírovej (H2IBA3):

Od vzniku tejto kyseliny dochádza k interakcii medzi katiónom sodíka (Na+1) zásaditého oxidu a siričitanového aniónu (SO3-2) kyseliny za vzniku siričitanu sodného (Na2IBA3):
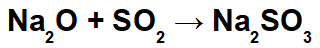
Reakcie so zásaditými oxidmi a amfotérnymi oxidmi
Amfotérne oxidy sú látky, ktoré vykazujú dvojaké chemické správanie: v prítomnosti kyslej látky sa správa ako zásaditý oxid; v prítomnosti látky zásaditej povahy sa správa ako kyslý oxid.
Takže keď a zásaditý oxid reaguje s amfotérnym oxidombude sa správať ako kyslý oxid, ktorý v prítomnosti vody vytvorí anorganickú kyselinu. Reakciou medzi aniónom anorganickej kyseliny a katiónom zásaditého oxidu vznikne soľný produkt.
Príklad: Oxid draselný a oxid chrómu III
V tejto reakcii máme ako reaktanty oxid draselný (K2O) a oxid chrómový (Cr2O3). Je pozoruhodné, že spočiatku, keď amfotérny oxid interaguje s vodou, dochádza k tvorbe chromozomálnej kyseliny (2HCrO2):

Od vzniku tejto kyseliny dochádza k interakcii medzi draselným katiónom (K+1) zásaditého oxidu a chromitového aniónu (SO3-2) kyseliny za vzniku chromitanu draselného (2KCrO2):

Od mňa, Diogo Lopes Dias
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/reacoes-com-oxidos-basicos.htm
