Koloidy, koloidné roztoky alebo koloidný systém sú zmesi, ktoré majú vzhľad roztoku, to znamená homogénnej zmesi. Ale v skutočnosti sú to heterogénne zmesi.
Je to tak preto, lebo hoci to nie je zrejmé voľným okom, rozdiel v koloidných zmesiach možno pozorovať pri použití nástrojov, ako je mikroskop.
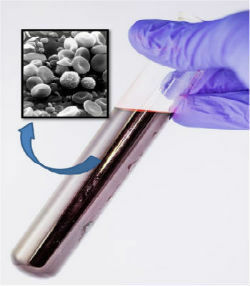 Krv, aj keď sa javila ako homogénna, pomocou mikroskopu sme pozorovali, že je zložená z niekoľkých zložiek.
Krv, aj keď sa javila ako homogénna, pomocou mikroskopu sme pozorovali, že je zložená z niekoľkých zložiek.
Koloidy sú prítomné v našom každodennom živote. Oni sú príklady koloidov: hydratačný krém, jogurt, mlieko, krv, farbivá a džem.
Z tohto dôvodu niektoré chemické výrobky naznačujú, že musia byť pred použitím pretrepané. Toto sa musí urobiť, aby sa spojili koloidné častice.
Koloidné zmesi sa zároveň prirodzene neusadzujú. Ak dáme do nádoby koloid, častice sa neusadzujú na dne. Tiež sa nedajú filtrovať.
Veľkosť častíc prítomných v koloidoch je medzi 1 a 100 nanometrami (1 nanometer zodpovedá 1 milióntine milimetra).
Všetko mimo tohto rozsahu je homogénne alebo heterogénne zmesi.
Homogénne zmesi sa považujú za skutočné riešenia. Jeho častice sú menšie ako 1 nanometer. Heterogénne zmesi majú častice väčšie ako 100 nanometrov.
Naučiť sa viac o Chemické roztoky a Separácia zmesí.
Aké sú vaše vlastnosti?
Zložky koloidov sa nazývajú rozptýlené a dispergačný prostriedok. Množstvo dispergačného prostriedku je vždy vyššie.
Zjavne predpokladajú homogénnu zmiešavaciu charakteristiku.
Jedným z príkladov je sneh vyšľahaný z bielkov: bielka v tekutej forme preberá úlohu rozptýlenej zložky.
Vzduch, ktorý spôsobil, že sa biela farba zmenila na penu, je disperznou zložkou, pretože na dosiahnutie tejto zmesi bolo potrebné viac vzduchu ako bielej farby.
Koloidy navyše umožňujú priechod svetla medzi nimi, čo neplatí pre homogénne zmesi.
Ak mierime baterkou s malým lúčom svetla na koloidnú zmes, je možné vidieť lúč svetla prechádzajúci celou nádobou, kde sa nachádza. Tak sa to volá Tyndallov efekt.
Rovnakým experimentom je tiež možné zistiť náhodný pohyb častíc v zmesi. Toto sa volá Brownovo hnutie.
Stručne povedané, vlastnosti koloidných systémov oni sú:
- Fázy zmesi nie sú ľahko rozlíšiteľné;
- Rozsah veľkosti častíc je 1 a 100 nanometrov;
- Tyndallov efekt;
- Prítomnosť dispergovaných častíc a dispergátorov;
- Neusadzujú sa prirodzene, ani sa nemôžu filtrovať;
- Brownovo hnutie.
Druhy koloidov
Koloidy sa klasifikujú podľa fyzikálneho stavu dispergovaných a dispergujúcich častíc.
Druhy koloidov sú: aerosól, emulzia, pena, gél a sol (tie, ktoré vyzerajú ako roztok). Získajte viac informácií o každom z nich:
Aerosól
Rozptýlený komponent: Tuhá alebo kvapalná
Dispergujúca zložka: plyn
Príklady: Dym, hmla, oblak, striekanie
Emulzia
Rozptýlený komponent: Kvapalina
Dispergujúca zložka: Kvapalina alebo tuhá látka
Príklady: Majonéza, maslo, syr, zmrzlina
Pena
Rozptýlený komponent: plyn
Dispergujúca zložka: Kvapalina alebo tuhá látka
Príklady: Šľahačka, biela v snehu, pena na holenie, popcorn
Gél
Rozptýlený komponent: Kvapalina
Dispergujúca zložka: pevné
Príklady: Želatína, silikagél, zubná pasta
slnko
Rozptýlený komponent: pevné
Dispergujúca zložka: Kvapalina alebo tuhá látka
Príklady: Perla, Rubín, Krv
Ak sa chcete dozvedieť viac, dozviete sa viac o metóde na oddeľovanie koloidných zmesí Odstreďovanie.



