Teplota topenia a teplota varu predstavujú teplotu, pri ktorej látka mení stav pri danom tlaku.
V prípade bodu topenia sa látka zmení z pevného skupenstva na kvapalné. Teplota varu sa vzťahuje na zmenu z kvapalného skupenstva do plynného skupenstva.
Napríklad ľad sa začne meniť na vodu v tekutej forme, keď je jeho teplota rovná 0 ° C. Teplota topenia vody je teda 0 ° C (pod tlakom 1 atmosféra).
Na prechod z kvapaliny na paru musí voda dosiahnuť teplotu 100 ° C. Bod varu vody je teda 100 ° C (pod tlakom 1 atmosféra).

Bod fúzie
Keď látka v tuhom stave dostane teplo, dochádza k zvýšeniu stupňa miešania jeho molekúl. Následne sa tiež zvyšuje jeho teplota.
Po dosiahnutí určitej teploty (teplota topenia) je miešanie molekúl také, že rozbijú vnútorné väzby medzi atómami a molekulami.
V tomto okamihu začne látka meniť svoj stav a ak bude naďalej prijímať teplo, prejde do tekutého stavu.
Počas Fúzia jeho teplota zostáva konštantná, pretože prijaté teplo sa používa výlučne na zmenu stavu.

Nazýva sa teplo na jednotku hmotnosti potrebné na zmenu fáz latentné teplo fúzie (Lf) a je charakteristikou látky.
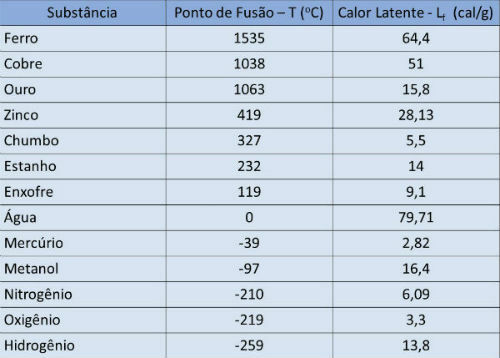
Teplota topenia a latentný tepelný stôl
V nasledujúcej tabuľke uvádzame teplotu topenia a latentné teplo niektorých látok atmosferický tlak.
Bod varu
THE vriaci vyznačuje sa rýchlym prechodom z kvapaliny do plynného skupenstva s tvorbou pár (bublín) vo vnútri kvapaliny.
Rovnako ako pri fúzii existuje teplota (teplota varu), pri ktorej sa daná látka mení z kvapalného na plynný stav.
Aby k tomu mohlo dôjsť, musí látka prijímať teplo. Počas celej zmeny fázy zostáva teplota konštantná.
latentné teplo z odparovanie (Ľv) je množstvo tepla na jednotku hmotnosti potrebné na to, aby látka mohla zmeniť fázu.
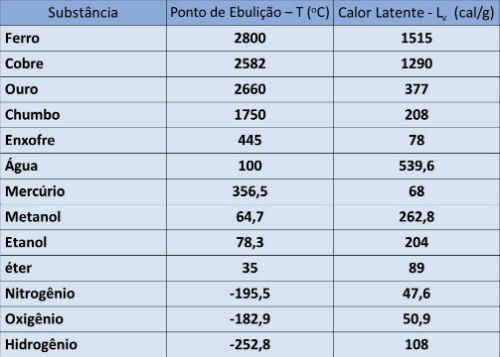
Bod varu a latentný tepelný stôl
V nasledujúcej tabuľke uvádzame teplotu varu a latentné odparovacie teplo niektorých látok pri atmosférickom tlaku.
Rušenie tlaku
Teplota topenia a teplota varu závisia od tlaku vyvíjaného na látku.
Všeobecne platí, že látky pri fúzii zväčšujú svoj objem. Táto skutočnosť znamená, že čím vyšší je tlak, tým vyššia je teplota, aby látka mohla zmeniť svoju fázu.
Výnimka sa vyskytuje u niektorých látok, vrátane vody, ktorá pri topení zmenšuje svoj objem. V takom prípade vyšší tlak zníži teplotu topenia.

Pokles tlaku spôsobí, že bod varu danej látky bude nižší, čo znamená, že látka bude vrieť pri nižšej teplote.
Napríklad na miestach nad morom voda vrie pri teplotách pod 100 ° C. Výsledkom je, že na týchto miestach sa varí oveľa dlhšie ako na miestach na hladine mora.
Prečítajte si tiež:
- Zmeny fyzikálneho stavu
- Teplomerové váhy
- Termometrické váhy - cvičenia
- Fyzikálne stavy vody
- Fázový diagram
- Tuhnutie
- Kondenzácia
- Koligatívne vlastnosti
- Periodické vlastnosti
- Odparovanie
- Cvičenia z periodickej tabuľky