Otázky týkajúce sa chemické rovnováhy v Enem sú veľmi opakujúce sa. Z tohto dôvodu sme vytvorili tento materiál, ktorý prináša najdôležitejšie témy týkajúce sa tohto odvetvia fyzikálnej chémie obsiahnuté v Národnej skúške na strednej škole (Enem).
Z problémov týkajúcich sa chemickej rovnováhy máme rovnovážnu konštantu z hľadiska koncentrácie v mol / L a z hľadiska tlaku, iónová rovnovážna konštanta, ionizačná konštanta, rovnovážny posun, pH a pOH, hydrolýzna konštanta, pufor a konštanta rozpustnosť.
Spomedzi predmetov opísaných vyššie sa niektoré z nich v Enemovi dostávajú do popredia:
Posun vyváženia
Ionizačná konštanta
pH
hydrolýza soľným roztokom
Video lekcia o chemickej rovnováhe na Enem
1. Rovnovážny posun v Enem
1.1- (Enem 2015) Hypoxia alebo výšková choroba spočíva v zníženom obsahu kyslíka (O2) v arteriálnej krvi tela. Z tohto dôvodu mnoho športovcov pociťuje pri cvičení vo vysokých nadmorských výškach nepohodlie (bolesti hlavy, závraty, dýchavičnosť). Za týchto podmienok dôjde k zníženiu koncentrácie okysličeného hemoglobínu (HbO2) v rovnováhe v krvi, podľa vzťahu:
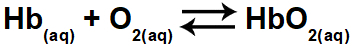
Zmena koncentrácie okysličeného hemoglobínu v krvi nastáva z dôvodu:
a) zvýšenie krvného tlaku.
b) zvýšenie telesnej teploty.
c) znižovanie teploty prostredia.
d) pokles parciálneho tlaku kyslíka.
e) zníženie množstva červených krviniek.
Okysličený hemoglobín (HbO2) sa nachádza v reaktantoch (na pravej strane) rovnice. Cvičenie sa pýta, ktorá z možností by viedla k zmene okysličeného hemoglobínu v krvi, to znamená, že by to posunulo rovnováhu doľava alebo doprava.
a) Falošné. Zvýšený prietok krvi nemá nič spoločné so zvýšeným krvným tlakom.
b) Falošné. Teplota nezmení poskytnuté vyváženie.
c) Falošné. Teplota nezmení poskytnuté vyváženie.
d) Pravda. Zníženie parciálneho tlaku kyslíka znižuje množstvo okysličeného hemoglobínu a posúva rovnováhu doľava.
e) Falošné. Pokles počtu červených krviniek spôsobí pokles počtu hemoglobínov aj okysličených hemoglobínov.
1.2- (Enem 2011) Nealkoholické nápoje sa stávajú čoraz viac cieľmi politík v oblasti verejného zdravia. Lepiace výrobky obsahujú kyselinu fosforečnú, látku škodlivú pre fixáciu vápnika, minerál, ktorý je hlavnou zložkou zubnej matrice. Kaz je dynamický proces nerovnováhy v procese zubnej demineralizácie, straty minerálov v dôsledku kyslosti. Je známe, že hlavnou zložkou zubnej skloviny je soľ nazývaná hydroxyapatit. Sóda v dôsledku prítomnosti sacharózy znižuje pH biofilmu (bakteriálneho plaku) a spôsobuje demineralizáciu zubnej skloviny. Slinným obranným mechanizmom trvá 20 až 30 minút, kým sa normalizuje úroveň pH a zub sa remineralizuje. Nasledujúca chemická rovnica predstavuje tento proces:

Ak vezmeme do úvahy, že človek konzumuje nealkoholické nápoje každý deň, môže dôjsť k procesu zubnej demineralizácie v dôsledku zvýšenia koncentrácie:
a) OH-, ktorý reaguje s iónmi Ca2+, posun rovnováhy doprava.
b) H+, ktorý reaguje s hydroxylovými skupinami OH-, posun rovnováhy doprava.
c) OH-, ktorý reaguje s iónmi Ca2+, pričom sa rovnováha posúva doľava.
d) H+, ktorý reaguje s hydroxylovými skupinami OH-, pričom sa rovnováha posúva doľava.
e) Ca2+, ktorý reaguje s hydroxylovými skupinami OH-, pričom sa rovnováha posúva doľava.
Správna odpoveď: Písmeno B
Rozhodnutie
Proces demineralizácie posúva rovnováhu doprava. Keď človek pije sódu, prijíma kyslý materiál, to znamená zvyšuje množstvo H+ v strede. H+ rýchlo interaguje s OH- rovnováhy, zníženie množstva OH-. Týmto spôsobom sa rovnováha posunie doprava, čím sa zub demineralizuje.
1.3 - (Enem-2013) Jedným z krokov úpravy vody je dezinfekcia, pričom najpoužívanejšou metódou je chlórovanie. Táto metóda spočíva v rozpustení plynného chlóru v roztoku pod tlakom a jeho aplikácii na vodu, ktorá sa má dezinfikovať. Jedná sa o rovnice chemickej reakcie:

Dezinfekčný účinok je riadený kyselinou chlórnatou, ktorá má dezinfekčný potenciál asi 80-krát väčší ako chlórnanový anión. Hodnota pH média je dôležitá, pretože ovplyvňuje mieru ionizácie kyseliny chlórnej. Aby bola dezinfekcia účinnejšia, musí sa pH upravovanej vody blížiť k:
a) 0
b) 5
c) 7
d) 9
e) 14
Správna odpoveď: Písmeno B
Podľa textu najlepšie dezinfekčne pôsobí látka HClO. Preto každý výklad a záver musia smerovať k spôsobu získania tejto látky.
Látka HClO je prítomná v druhej rovnováhe, takže zaujímavou taktikou je posunúť túto rovnováhu doľava. Za to podľa princíp Le Chatelier, máme možnosť zvýšiť množstvo H+ (pridanie kyslej látky, pH nižšie ako 7) alebo zvýšenie množstva Cl-.
Je pozoruhodné, že v prvej rovnici existuje ďalšia chemická rovnováha, ktorá obsahuje druhy HClO-, ktorý má afinitu k H+, pričom sa rovnováha posúva doľava. Toto je krok, ktorý nechceme.
Preto musíme použiť kyslé pH (pod 7). Toto pH by však nemalo byť príliš kyslé, aby sa zabránilo použitiu veľkého množstva katiónov H.+ v strede.
Pozri tiež:Chemická rovnováha v jaskyniach
2. pH a hydrolýza soľného roztoku v Enem
2.1- (Enem-2017) Niekoľko prírodných produktov je možné získať z rastlín procesom extrakcie. Lapachol patrí do triedy naftochinónu. Jeho štruktúra má enolhydroxylovú skupinu (pKa = 6,0), ktorá umožňuje izolovať túto zlúčeninu z ipe pilín extrakciou adekvátnym roztokom, po ktorej nasleduje jednoduchá filtrácia. Uvažujme, že pKa = -log Ka a že Ka je kyslá konštanta lapacholovej ionizačnej reakcie.

Ktoré riešenie by sa malo použiť na efektívnejšiu extrakciu lapacholu z pilín ipê?
a) Roztok Na2CO3 za vzniku lapacholovej soli.
b) Tlmivý roztok kyselina octová / octan sodný (pH = 4,5).
c) roztok NaCI za účelom zvýšenia iónovej sily média.
d) Na roztok2IBA4 za vzniku iónového páru s lapacholom.
e) roztok HCI, aby sa extrahoval pomocou acidobázickej reakcie.
Vyhlásenie naznačuje, že pKa látky je 6,0. Táto hodnota pKa sa musí použiť vo výraze pKa:
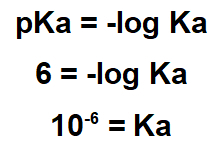
Pretože váš Ka je malý, lapachol je kyslá látka, takže na jeho odstránenie je užitočné použiť zásaditú látku.
a) Pravda. Soľ je zásaditá, pretože pochádza zo silnej bázy (pretože je z rodiny IA), a CO3 pochádza zo slabej kyseliny (H2CO3).
b) Falošné. Tlmivý roztok je kyslý a potrebujeme bázu.
c) Falošné. NaCl je neutrálna soľ, pretože pochádza zo silnej bázy (pretože je z rodiny IA), a Cl pochádza zo silnej kyseliny (HCl).
d) Falošné. O2IBA4 je neutrálna soľ, pretože Na pochádza zo silnej bázy (pretože je z rodiny IA), a SO4 pochádza zo silnej kyseliny (H2IBA4).
je to falošné. HCl je kyselina a potrebujeme bázu.
2.2- (Enem- 2014) S cieľom minimalizovať dopady na životné prostredie brazílska legislatíva určuje, že chemické zvyšky uvoľňované priamo do prijímajúceho tela majú pH medzi 5,0 a 9,0. Vodný kvapalný odpad generovaný priemyselným spôsobom má koncentráciu hydroxylových iónov rovnú 1,0.10-10 mol / l. V súlade s právnymi predpismi chemik oddelil nasledujúce látky, ktoré sú dostupné v sklade spoločnosti: CH3COOH, Na2S04, CH3OH, K.2CO3 a NH4Cl.
Teraz neprestávajte... Po reklame je toho viac;)
Ktorá látka by sa mohla použiť na úpravu pH, aby sa zvyšok mohol uvoľniť priamo do prijímajúceho tela?
a) CH3COOH
b) v2IBA4
c) CH3oh
d) K.2CO3
e) NH4Cl
Správna odpoveď: Písmeno D
Rozhodnutie
Krok 1: Stanovte pH zvyšku.
Toto cvičenie naznačuje, že zvyšok má koncentráciu hydroxidu rovnú 10-10.
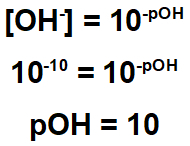
Preto môžeme vypočítať pH tohto zvyšku:

Z vyššie uvedeného vyplýva, že zvyšok má kyslý charakter, pretože jeho pH je nižšie ako 7. Na jej zneškodnenie je teda nevyhnutné použiť látku základného charakteru.
Krok 2: Určte charakter každej soli, aby ste určili, ktorá z nich je zásaditá, ako CH3COOH (alternatíva a) je kyselina a CH3OH (alternatíva c) je alkohol organickej triedy s kyslým charakterom.
b) Neutrálna soľ, pretože Na pochádza zo silnej bázy (pretože je z rodiny IA) a SO4 pochádza zo silnej kyseliny (H2IBA4).
d) Zásaditá soľ, pretože K pochádza zo silnej bázy (pretože je z rodiny IA), a CO3 pochádza zo slabej kyseliny (H2CO3).
e) Kyselinová soľ, ako NH4 pochádza zo slabej bázy (NH4OH) a Cl pochádza zo silnej kyseliny (HCl).
2.3- (Enem- 2014) Vedec si všimne, že štítok na jednej z nádob, v ktorej uchováva koncentrát tráviacich enzýmov, je nečitateľný. Nevie, ktorý enzým obsahuje sklo, ale má podozrenie, že ide o žalúdočnú proteázu, ktorá v žalúdku pracuje trávením bielkovín. S vedomím, že trávenie v žalúdku je kyslé a črevo je zásadité, zostaví s jedlom päť skúmaviek rôzne, pridajte enzýmový koncentrát do roztokov so stanoveným pH a počkajte, či enzým v nejakom účinkuje ich. Skúmavka, v ktorej musí enzým pôsobiť, aby naznačila, že hypotéza výskumníka je správna, je tá, ktorá obsahuje:
a) kocka zemiakov v roztoku s pH = 9.
b) kus mäsa v roztoku s pH = 5.
c) varený vaječný bielok v roztoku s pH = 9.
d) časť rezancov v roztoku s pH = 5.
e) maslová guľôčka v roztoku s pH = 9.
Správna odpoveď: Písmeno B
Cvičenie vyžaduje od študenta dobrú interpretáciu a koreláciu s biochemickými znalosťami potravín. Informuje, že vedec si myslí, že enzým je tráviaci, pôsobí pri kyslom pH a pôsobí na bielkoviny (pretože ide o proteázu).
Ak tento enzým pôsobí v kyslom prostredí, musí byť pH nižšie ako 7. Mäso sa skladá z bielkovín, zatiaľ čo cestoviny zo sacharidov. Správna odpoveď je teda alternatíva b.
2.4- (Enem- 2012) Gazdiná nechtiac pustila z rozmrazovania ryby do chladničky vodu, ktorá vo vnútri prístroja zanechala silný a nepríjemný zápach. Je známe, že charakteristický zápach rýb je spôsobený amínmi a že tieto zlúčeniny sa správajú ako zásady. V tabuľke sú uvedené koncentrácie vodíka niektorých materiálov nachádzajúcich sa v kuchyni, ktoré domáca pani uvažuje použiť pri čistení chladničky.

Ktoré z uvedených materiálov sú vhodné na zmiernenie tohto zápachu?
a) Alkohol alebo mydlo
b) Citrónová šťava alebo alkohol
c) Citrónová šťava alebo ocot
d) Citrónová šťava, mlieko alebo mydlo
e) Mydlo alebo sóda / sóda
Správna odpoveď: Písmeno C.
Rozhodnutie
Cvičenie navrhuje problémovú situáciu, v ktorej má chladnička ženy v domácnosti silný zápach spôsobený látkou základnej povahy. Je teda otázne, ktoré materiály by boli zaujímavé pri riešení tohto problému.
Na neutralizáciu zásady je potrebné použiť materiál kyslého charakteru alebo s pH nižším ako 7. Ako cvičenie poskytlo hodnoty koncentrácií H+ materiálov stačilo použiť každý z nasledujúcich výrazov:

Takto:
Šťava: pH = 2
Mlieko: pH = 6
Ocot: pH = 3
Alkohol: pH = 8
Mydlo: pH = 12
Sud: pH = 12
Materiály s kyslým charakterom sú šťava, ocot a mlieko. Iba alternatíva c teda prináša materiály kyslého charakteru.
3. Rovnovážna konštanta v Enem
3.1- (Enem-2016) Po úplnom opotrebení môžu byť pneumatiky na výrobu energie spálené. Medzi plynmi generovanými pri úplnom spaľovaní vulkanizovaného kaučuku sú niektoré znečisťujúce látky, ktoré spôsobujú kyslé dažde. Aby sa zabránilo ich úniku do atmosféry, môžu sa tieto plyny prebublávať do vodného roztoku obsahujúceho vhodnú látku. Zvážte informácie o látke uvedené v nasledujúcej tabuľke:

Z látok uvedených v tabuľke je ten, ktorý je schopný najúčinnejšie odstraňovať znečisťujúce plyny, a)
a) fenol.
b) pyridín.
c) metylamín.
d) hydrogenfosforečnan draselný.
e) hydrogénsíran draselný.
Správna odpoveď: Písmeno D
Rozhodnutie
Cvičenie predstavuje problémovú situáciu, v ktorej znečisťujúce plyny podporujú kyslé dažde. Potom sa pýta, ktoré z uvedených látok by bolo zaujímavé neutralizovať tieto plyny a následne sa vyhnúť kyslým dažďom.
Aby sa zabránilo kyslým dažďom, musia sa kyslé plyny neutralizovať zásaditým roztokom. Látky s touto charakteristikou sú tie, ktoré prednostne uvoľňujú OH skupiny- v strede. V tabuľke sú pyridín, metylamín a hydrogénfosforečnan draselný základné látky.
Aby sme teda mohli určiť látku schopnú účinnejšie odstraňovať znečisťujúce plyny, musíme analyzovať hodnotu ionizačnej konštanty. Čím väčšia je konštanta, tým vyššia je schopnosť uvoľňovať OH-. Takže hydrogenfosforečnan draselný v tomto prípade je to najvhodnejšia látka.
3.2- (Enem-2015) Niekoľko kyselín sa používa v priemyselných odvetviach, ktoré likvidujú svoje odpadové vody vo vodných útvaroch, ako sú napríklad rieky a jazerá, čo môže mať vplyv na rovnováhu životného prostredia. Na neutralizáciu kyslosti sa môže do odtoku vo vhodných množstvách pridať soľ uhličitanu vápenatého, pretože produkuje hydrogenuhličitan, ktorý neutralizuje vodu. Uvádzajú sa rovnice zapojené do procesu:

Na základe hodnôt rovnovážnych konštánt reakcií II, III a IV pri 25O C, aká je číselná hodnota rovnovážnej konštanty reakcie I?
a) 4,5 x 10-26
b) 5x10-5
c) 0,8 x 10-9
d) 0,2 x 105
e) 2,2 x 1026
Správna odpoveď: Písmeno B
Rozhodnutie
Toto cvičenie zahŕňa neustálu ionizáciu. Spočiatku je nevyhnutné pochopiť, že rovnica I je vlastne výsledkom (súčtom) rovníc II, III a IV. Preto, aby sme iniciovali uznesenie, musíme použiť princípy Hessov zákon.
Krok 1: Použitie Hessovho zákona.
Invertovaním rovnice II a udržiavaním rovníc III a IV máme:
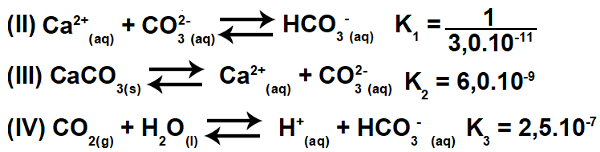
Môžeme teda pozorovať, že anión CO3-2 a katión H.+ bude eliminované a súčet rovníc bude mať za následok rovnicu I.
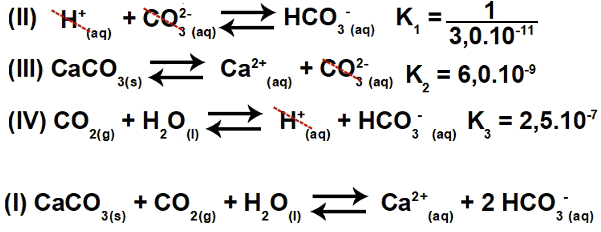
Krok 2: konštantný výpočet
Rovnovážna konštanta ionizačnej rovnice je vždy daná vynásobením konštánt ostatných rovníc:

Podľa mňa. Diogo Dias


