O prací prášok je to čistiaci prostriedok, ktorý je súčasťou každodenného života veľkej časti populácie, pretože sa používa na uľahčenie prania odevov. Je to produkt, ktorý nahradil barové mydlo, pretože ľudia si zvykli pri praní všeobecne trieť svoje oblečenie o oblečenie.

Barové mydlo sa stále často používa napríklad pri umývaní riadu
Práškové mydlo bolo prvýkrát vyrobené v roku 1946, po niekoľkých pokusoch o uľahčenie používania tyčového mydla. Jedným z pokusov bolo vyrobiť mydlo vo vločkách alebo granulách. Tieto pokusy však neboli úspešné, pretože mydlo interaguje s iónmi prítomnými v tvrdej vode, čo hlavne zhoršuje čistiaci účinok.
Prečo by sme nemohli takto nazvať prací prášok?
Z chemického hľadiska nemôžeme takto nazvať prací prášok. Ak sa pozrieme na obal týchto výrobkov, uvidíme, že sa v nich hovorí o práčkach, nie o pracích práškoch. Je správne to nazvať Práškový prací prostriedok, pretože jeho chemické zloženie je odlišné od zloženia mydla.
Chémia pracieho prášku, alebo lepšie pracieho prášku, je založená na základnom rozdiele medzi mydlom a pracím prostriedkom. Pozri definíciu a chemické vlastnosti týchto materiálov:
a) Čistiace prostriedky:
Jedná sa o chemické látky, ktoré majú veľmi dlhé reťazce (veľké množstvo uhlíkov) tvorené iba atómami uhlíka a vodíka, ktoré konfigurujú to, čo nazývame regióny nepolárny. Na konci tohto dlhého reťazca sa tiež nachádza polárna skupina.
Polárna časť pracieho prostriedku je spôsobená prítomnosťou sulfonátovej skupiny, to znamená atómu síry interagujúceho s tri atómy kyslíka alebo fosfátová skupina, ktorá má atóm fosforu interagujúci s tromi atómami kyslík. Pozrite si znázornenie štruktúry čistiaceho prostriedku:
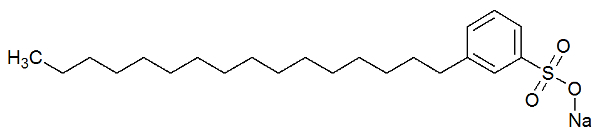
Štrukturálny vzorec pracieho prostriedku
Polárna časť detergentu (tvorená síranom sodným) je schopná interagovať s molekulami vody. Nepolárna časť (tvorená iba uhlíkmi a vodíkmi) interaguje s molekulami tuku. Vďaka detergentu teda tuk interaguje s vodou a vytvára emulziu.
b) Mydlá
sú soli karboxylové kyseliny vznikol chemickou reakciou medzi tukmi a silnými zásadami, ako je NaOH. Pozrite si znázornenie chemickej štruktúry mydla:
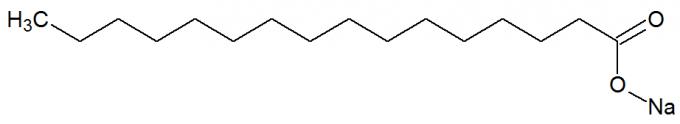
Štrukturálny vzorec mydla
Majú tiež dlhé uhlíkové reťazce s nepolárnou a polárnou časťou. Týmto spôsobom je nepolárna časť (tvorená iba uhlíkmi a vodíkmi) mydla schopná interagovať s tuky a ich polárna časť (tvorená skupinou COONa) s vodou vytvára emulzie, napríklad detergenty.
Tento text sa zameriava na chémiu „mydlového“ prášku, alebo skôr chemické zloženie práškového pracieho prostriedku, uvádzame všetky chemické látky, ktoré sú súčasťou jeho zloženia, ako aj dôležitosť každej z nich:
Chemické zloženie práškového čistiaceho prostriedku
aniónový tenzid (ako je alkylbenzénsulfonát sodný a alkylétersulfonát sodný). Viažu sa na molekulu tuku aj na molekulu vody, čím odstraňujú tuk z tkaniva;
Enzýmy: Na odstránenie škvŕn sa používajú lipázy a proteázy. Je to tak preto, lebo chemicky sú enzýmy biochemickými katalyzátormi, ktoré podporujú transformáciu zložitých molekúl na jednoduchšie molekuly. Menšie molekuly sa tak dajú ľahšie odstrániť z odevu;
Bielidlo (perboritan sodný): Pôsobí oxidáciou, redukciou alebo enzymatickým účinkom. Vo vode produkuje peroxid vodíka, ktorý je silným oxidačným činidlom. Chemicky reagujú s pigmentom odevu, modifikujú štruktúru a vedú k zmene farby;
Optické blokátory: sú to látky, ktoré absorbujú ultrafialové žiarenie alebo ultrafialové svetlo a krátko potom vyžarujú modré fluorescenčné svetlo, ktoré maskuje napríklad žltkastú farbu oblečenia;
Vône: Sú to esencie, ktoré po praní zanechávajú na odevoch príjemný zápach. Je pozoruhodné, že vône sú esencie (patria k funkcii esteru);
Farbivá: Látky použité na zafarbenie produktu;
Sekvestračné a chelatačné činidlá: EDTA (kyselina etyléndiamíntetraoctová) je príkladom sekvestranta. Interakujú s iónmi vápnika, horčíka a železa prítomnými hlavne v tvrdej vode, čo neumožňuje interakciu žiadnej zložky pôsobiacej pri čistení, ako je napríklad povrchovo aktívna látka.
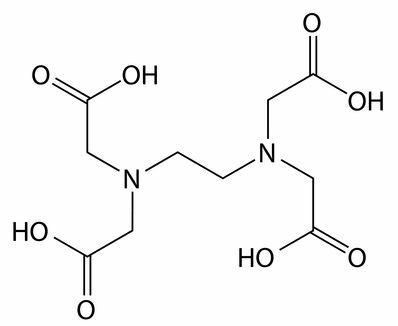
Štrukturálny vzorec sekvestrantu EDTA
Podľa mňa. Diogo Lopes Dias
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/quimica-sabao-po.htm

