Allotropia je jav, ktorý nastáva, keď má rovnaký chemický prvok vlastnosť vytvárať viac ako jednu jednoduchú látku.. Tieto alotropické odrody sa môžu líšiť z dôvodu počtu atómov prvku, ktoré sú navzájom spojené v molekule, alebo z dôvodu usporiadania atómov v kryštálovej mriežke.
Jedným z prvkov, ktoré majú alotropické odrody, je fosfor (P), najbežnejší je biely fosfor to je červený fosfor. Tieto dva fosforové alotropy sa nelíšia odlišným priestorovým usporiadaním, pretože obidve sú v zásade tvorené štvorbokými molekulami, ale množstvo atómov fosforu je u každého odlišné.
Pozrite sa na zloženie a hlavné charakteristiky bieleho a červeného fosforu:
- Biely fosfor:
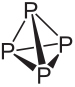
Molekulárny vzorec bieleho fosforu je P4, čo znamená, že jeho molekuly sú tvorené štyrmi atómami fosforu.

Tento typ fosforu je extrémne reaktívny, hlavne kvôli napätiu v uhloch 60 ° medzi jeho väzbami. Je tak reaktívny, že ho treba skladovať vo vode, aby neprišiel do styku so vzduchom a nevybuchol. Pri manipulácii s ním treba postupovať veľmi opatrne, pretože pri požití spôsobuje vážne popáleniny a otravu pokožkou (iba 0,1 g požitého bieleho fosforu môže viesť k smrti).
Ako môžete vidieť nižšie, biely fosfor je biela tuhá látka podobná vosku.

Biely fosfor skladovaný vo vode tak, aby neprišiel do styku so vzduchom *
Ak sa biely fosfor zahreje bez prítomnosti vzduchu, zmení sa na červený fosfor.
- červený fosfor:
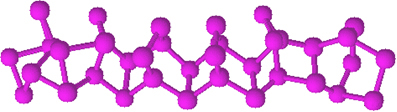
Červený fosfor nemá určenú štruktúru, ale existujú dôkazy, že ide o makromolekuly tvorené väzbou uvedených tetraedrických štruktúr (P4), v zastúpení: Pč.
Je oveľa menej reaktívny ako biely fosfor, môže sa však pri trení vznietiť. Preto sa používa na bočných plochách zápalkových škatúľ. Keď špáradlo potrieme o povrch škatule, zápalka sa zapáli a zasa zapáli vysoko horľavý materiál na hlave špáradla.
V niektorých krajinách je zápalka umiestnená na hlave špáradla vo forme P.4s3.
Červený fosfor je amorfný prášok, to znamená, že nemá kryštalickú štruktúru a má tmavočervenú farbu, ako je uvedené nižšie:

Prášok červeného fosforu.
* Autorstvo obrázkov patrí W. Oelen a ona sa dá nájsť tu.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Zdroj: Brazílska škola - https://brasilescola.uol.com.br/quimica/alotropia-fosforo.htm

