Ako je vysvetlené v texte „Typy intermolekulárnych síl“, molekuly látok v troch fyzikálnych stavoch (tuhý, kvapalný a plynný) sú priťahované jednou z intermolekulárnych síl.
Tri známe medzimolekulové sily sú: indukovaný dipól - indukovaný dipól, permanentný dipól - permanentný dipól a vodíkové väzby. Medzi nimi je najsilnejšia vodíková väzba. Niektorí autori zvykli túto medzimolekulárnu silu označovať ako vodíkové väzby; správny termín akceptovaný IUPAC je však „vodíková väzba“.
Tento typ interakcie nastáva, keď má molekula vodík naviazaný na fluór, dusík alebo kyslík, čo sú silne elektronegatívne atómy.

Vodíková väzba je extrémnym príkladom permanentnej dipólovej permanentnej dipólovej väzby. Pre vodík molekuly predstavuje kladný pól, ktorý sa viaže na jeden z atómov fluóru, kyslíka alebo dusíka inej molekuly, ktoré tvoria ich záporný pól.
Za normálnych okolností sa intermolekulárne väzby vyskytujú s látkami v kvapalnom a pevnom skupenstve. Pretože je to veľmi príťažlivá sila príťažlivosti, vyžaduje sa na jej rozbitie veľmi vysoká energia.
Látka, ktorá má túto medzimolekulovú silu, je sama voda. Všimnite si, ako sa to deje na ilustrácii nižšie:
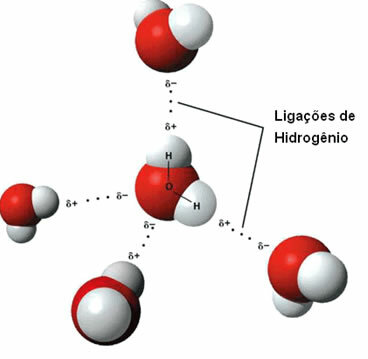
Upozorňujeme, že každá molekula vody je priestorovo obklopená štyrmi ďalšími molekulami vody s väzbami vodíka nastáva väzbou medzi vodíkom jednej molekuly (kladný pól) s kyslíkom druhej (pól negatívny).
Vodíkové väzby vysvetľujú rôzne javy v prírode, pozri nasledujúce príklady:
- Skutočnosť, že ľad pláva na vode: Ľad je menej hustý ako voda a následne na ňom pláva. Je to tak preto, lebo zatiaľ čo v kvapalnom stave sú vodíkové väzby, ktoré sa vyskytujú medzi molekulami vody, usporiadané v dezorganizovanom tvare, vodíkové väzby v molekuly ľadu sú viac rozmiestnené a usporiadané a vytvárajú tuhú šesťuholníkovú štruktúru, vďaka ktorej molekuly zaberajú oveľa väčší priestor, ako by boli, keby boli v takom stave. tekutý.

Teraz neprestávajte... Po reklame je toho viac;)
To je dokonca dôvod, prečo ak dáme vodu do celého objemu fľaše a dáme ju neskôr do chladiča, jej objem sa zväčší a fľaša praskne.
Teda bude rovnaké množstvo molekúl na jednotku objemu, čo znižuje hustotu, podľa vzorca hustoty: d = m / v. Medzi vytvorenými šesťuholníkmi budú prázdne medzery, ktoré znižujú hustotu tejto látky.
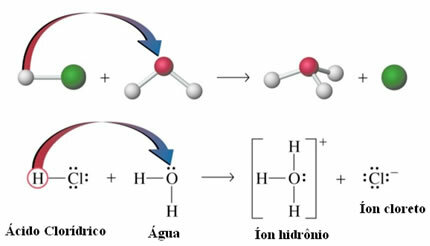
- Kyselinová ionizácia: Aj keď sú vodíkové väzby približne desaťkrát slabšie ako kovalentné väzby; za určitých okolností sa im podarí prelomiť kovalentné väzby. Napríklad v prípade uvedenom nižšie je kyselina chlorovodíková rozpustená vo vode. Kyslík vo vode priťahuje vodík viazaný na chlór kyseliny viac ako samotný chlór, čo vedie k vzniku iónov hydrónia (H3O+) a chlorid (Cl-). Tento jav sa nazýva ionizácia:
- Povrchové napätie vody: molekuly na povrchu kvapaliny sú priťahované vodíkovými väzbami iba s molekulami vedľa nich a dole, pretože hore nie sú žiadne molekuly. Molekuly, ktoré sú pod povrchom, na druhej strane uskutočňujú tento typ väzby s celkovými molekulami smeroch, výsledkom je tvorba akéhosi filmu alebo tenkej vrstvy na povrchu vody, ktorá zahŕňa.
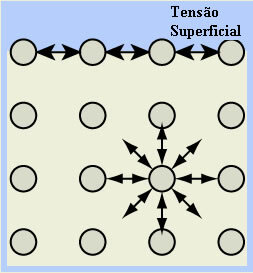
To vysvetľuje skutočnosť, že na ňom môže zostať hmyz, a tiež fenomén sférického tvaru vodných kvapiek.

Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Vodíkové väzby“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/ligacoes-hidrogenio.htm. Sprístupnené 27. júna 2021.
Chémia

Znečistenie vody, fyzikálne aspekty vody, chemické aspekty vody, biologické aspekty vody, priemyselný odpad, ťažké kovy, pitná voda, organické látky, zákal vody, odpadové vody.

