entalpia je množstvo energie v danej reakcii, variácia entalpie sa vzťahuje na pôvod tejto energie. Napríklad, ak energia pochádza z fúznej reakcie (prechod látky z pevného skupenstva do kvapaliny), budeme mať fúznu entalpiu. Existuje niekoľko typov entalpie, pozri nižšie:
Entalpia formácie: je variácia entalpie overená pri tvorbe 1 molu molekúl danej látky v štandardnom stave (za podmienok okolia (25 ° C a 1 atm) a v stabilnejšom alotropnom stave). Za túto látku považujme vodu:
H2 (g) + ½ O2 (g) → 1 H2O (l) ∆Hf = -68,3 kcal / mol
Entalpia tvorby vody (H2O) je -68,3 Kcal / mol, táto hodnota zodpovedá získaniu 1 mol H2O (l) prostredníctvom prvkov v štandardnom stave.
Neutralizačná entalpia: hodnota pochádzajúca z tepla absorbovaného pri neutralizácii 1 mol OH- (aq) s 1 mol H + (aq), pokiaľ sú v zriedených vodných roztokoch.
H+ (aq) + OH- (aq) → H2(1) ∆H = -13,8 kcal / mol
entalpia rozpúšťaniaje teplo zistené pri rozpustení 1 molu rozpustenej látky v rozpúšťadle v množstve dostatočnom na získanie zriedeného roztoku.
HCl (g) + H2O (1) → H30+(aq) + Cl- (aq) ∆H = -18,0 Kcal / mol
Vyššie uvedená rovnica predstavuje entalpiu rozpúšťania plynného chlorovodíka.
Teraz neprestávajte... Po reklame je toho viac;)
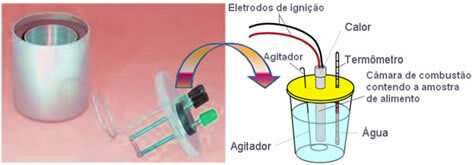
Entalpia horenia: je teplo absorbované pri úplnom spálení 1 molu látky za podmienok okolia (25 ° C a 1 atm). Spaľovaním sa uvoľňuje teplo, prebieha medzi palivom a okysličovadlom, palivom môže byť akákoľvek látka, hlavným oxidačným prostriedkom je kyslík.
1 CH4(g) +202(g) → CO2(g) + 2 H2O (1) ∆H = - 212,8 kcal / mol
Hodnota - 212,8 Kcal / mol sa týka spaľovania 1 mol CH metánu4g) pri okolitých podmienkach 25 ° C a tlaku 1 atm.
Entalpia tuhnutia: zodpovedá zmene entalpie v celkovom tuhnutí 1 molu látky pri tlaku 1 atm.
H2O (1) → H2O (s) ΔH = - 1,7 Kcal / mol
Entalpia kondenzácie: s odkazom na zmeny entalpie v celkovej kondenzácii 1 molu látky pri tlaku 1 atm.
H2O (v) → H2O (l) ΔH = - 10,5 kcal / mol
Entalpia fúzie: zmena entalpie v celkovej fúzii 1 molu látky pri tlaku 1 atm.
H2O (s) → H2O (l) ΔH = + 1,7 Kcal / mol
entalpia odparovania: zodpovedá zmene entalpie v celkovom odparení 1 molu látky pri tlaku 1 atm.
H2O (1) → H2O (v) ΔH = + 10,5 Kcal / mol
Líria Alves
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
SOUZA, Líria Alves de. „Zmeny entalpie v reakciách“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/variacao-entalpia-nas-reacoes.htm. Prístup k 28. júnu 2021.