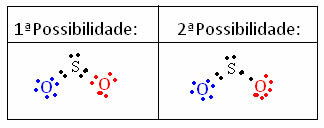
Kapacita, ktorú musia spojenia priťahovať elektrické náboje, je definovaná ako polarita, ktorá nadobúda odlišný charakter v závislosti na pripojení, kde je prítomné.
Čo sa týka iónovej a kovalentnej väzby, ktorá by bola polárna alebo nepolárna?
Iónové zlúčeniny sú nabité elektrickými nábojmi: katiónmi a aniónmi, ktoré sa nazývajú kladný a záporný pól. Predstavujú ich značky δ + a δ-. Iónové látky reagujú s inými zlúčeninami v dôsledku prítomnosti týchto pólov, ktoré spôsobujú nestabilitu väzby. Príklad: z iónovej väzby atómov chlóru a sodíka vzniká zlúčenina chlorid sodný (Na + Cl-), všeobecne známa ako kuchynská soľ.
Stručne povedané: Každá iónová väzba je polárna väzba.
Kovalentné zlúčeniny sú väčšinou klasifikované ako nepolárne.
Pamätajte však: neznamená to, že každá kovalentná zlúčenina je nepolárna. Póly sú spojené s elektronegativitou, ak je kovalentná väzba medzi atómami rovnakej elektronegativity, väzba bude nepolárna, pretože nedochádza k tvorbe pólov.
Príklad: kovalentná zlúčenina C
H H H
│ │ │
H C ─ C ─ C ─ H
│ │ │
H H H
Upozorňujeme, že k väzbe dochádza medzi rovnakými prvkami, takže majú rovnakú stupnicu elektronegativity.
Teraz neprestávajte... Po reklame je toho viac;)
Líria Alves
Vyštudoval chémiu
Brazílsky školský tím
Pozrieť viac:
Nezabudnite na elektronegativitu
Zistite, ktoré prvky sú elektronegatívne
Všeobecná chémia - Chémia - Brazílska škola
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
SOUZA, Líria Alves de. „Polarita iónových a kovalentných väzieb“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/polaridade-das-ligacoes-ionica-covalente.htm. Sprístupnené 27. júna 2021.