Zvážte nižšie uvedenú všeobecnú reverzibilnú reakciu, kde malé písmená zodpovedajú vyváženým reakčným koeficientom a veľké písmená sú reaktanty a produkty sú všetky plynné:

Ak vezmeme do úvahy každý z reakčných smerov osobitne, sú ich rýchlosti vývoja (Td) dané:
* Priama reakcia: aA + bB → cC + dD
Všetkypriamy = K.priamy. [THE]The. [B]B
* Reverzná reakcia: cC + dD → aA + bB
Všetkyinverzný = K.obrátiť. [Ç]ç. [D]d
Chemická rovnovážna konštanta z hľadiska koncentrácie v množstve hmoty (K.ç) a z hľadiska parciálneho tlaku (K.P) bude dané vydelením Kpriamy od K.obrátiť.
Takže máme:
Kpriamy. [THE]The. [B]B = 1 → Kpriamy__ = __[Ç]ç. [D]d___
Kobrátiť. [Ç]ç. [D]d Kobrátiť [THE]The. [B]B
Byť, Kç =_Kpriamy_
Kobrátiť
Takže máme:
Kç =__[Ç]ç. [D]d___ alebo K.P =__(Praça)ç. (pD)d___ |
Kde p je parciálny tlak každej látky v rovnováhe.
Týmto spôsobom sa každá koncentrácia zvýši na exponent zodpovedajúci koeficientu príslušnej látky v reakcii a K.ç nemá jednotku *.
Okrem toho je potrebné zdôrazniť veľmi dôležitý aspekt v tomto výraze
tuhé zložky ani čisté kvapaliny by nemali byť zastúpené., pretože na tomto výraze sa zúčastňujú iba záležitosti, ktoré môžu trpieť rôznymi zmenami. Koncentrácia v množstve látky v tuhom stave je konštantná, a preto je už zahrnutá v hodnote samotného K.ç. To isté platí pre čisté kvapaliny, ako je voda. V skratke, na expresii sa podieľajú iba látky v plynnom stave a vo vodnom roztoku.Teraz neprestávajte... Po reklame je toho viac;)
Všimnite si nasledujúce príklady:
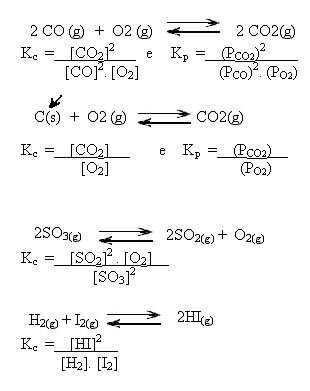
Hodnoty K.ç môže nám ukázať, či je koncentrácia reaktantov a produktov rovnaká alebo či je jedna vyššia ako druhá:
- ak Kç alebo K.P sa rovná jednej (K.ç = 1), to znamená, že koncentrácia reaktantov a produktov je rovnaká;
- ak je hodnota Kç alebo K.P byť vysokýTo znamená, že produkty sú vo väčšej koncentrácii, pretože v expresii K.ç výrobky sú v čitateľovi;
- ak je hodnota Kç alebo K.P je nízkyTo znamená, že činidlá sú vo vyššej koncentrácii, pretože v expresii K.ç činidlá sú v menovateli.
* K.ç a K.P sú to bezrozmerné čísla, teda čisté čísla, bez jednotky súvisiacej s veľkosťou alebo vzťahom medzi veľkosťami.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Rovnovážné konštanty Kc a Kp“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Prístup k 28. júnu 2021.