Princíp Le Chatelier: ak je sila použitá na systém v rovnováhe, má tendenciu sa znova upravovať, aby sa znížili účinky tejto sily.
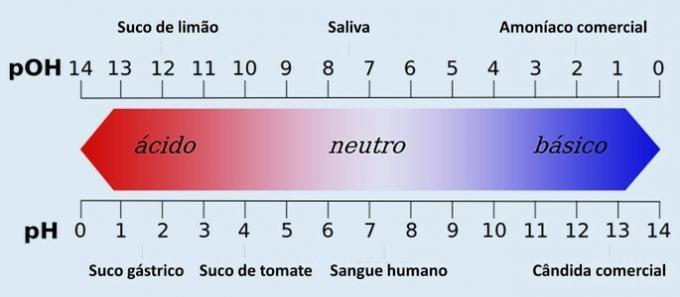
Zmeny kyslosti a zásaditosti pôsobia ako vonkajšie sily na chemické rovnováhy. Systém sa potom musí pohybovať, aby zmiernil účinky tejto sily. Pozrime sa na príklad faktora, ktorý môže zmeniť rovnováhu systému, koncentráciu.
2 CrO2-4 (aq) + 2 H+(tu) ↔ CrO2-7(tu)+ H2O (1)
Ak do tejto rovnováhy pridáme niekoľko kvapiek citrónu (kyslý roztok), presunie sa to doprava alebo doľava a podporí tvorbu jedného z produktov.
Je to tak preto, lebo touto akciou zvýšime množstvo iónov H + v jednom z členov rovnice. Ak k tomu dôjde v reaktantoch vľavo, rovnováha sa posunie doprava, aby sa vyvážila sama.
Reakciu je možné obrátiť, ak do systému pridáme zásaditý roztok NaOH. Prítomnosť iónov OH- spotrebúva ióny H + a rovnováha sa posúva doľava.
Záver: Keď je koncentrácia iónov (CrO2-7) prevažuje, rovnováha sa posúva doľava. Ak je koncentrácia iónov (CrO 2-4) prevažujú, rovnováha sa posúva doprava.
Teraz neprestávajte... Po reklame je toho viac;)
Líria Alves
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Princíp Le Chatelier“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/principio-le-chatelier.htm. Prístup k 28. júnu 2021.