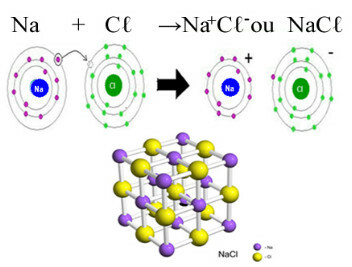
Joseph Lous Gay-Lussac (1778-1850) bol vedec, ktorý uskutočňoval dôležité štúdie o plynoch. Vykonal výrobu vody z reakcie medzi vodíkovými a kyslíkovými plynmi a overil ich vždy reagoval v pomere dvoch objemov vodíka k jednému objemu kyslíka za vzniku dvoch objemov Voda:
Vodík + kyslík → voda
1. experiment: 2 L 1 L 2 L
2. experiment: 4 L 2 L 4 L
3. experiment: 8 L 4 L 8 L
4. experiment: 16 L 8 L 160 L
Upozorňujeme, že pri všetkých experimentoch je pomer vždy rovnaký: 2: 1: 2.
Po niekoľkých experimentoch a analýzach si uvedomili, že to isté sa stalo aj pri iných druhoch reakcií medzi plynmi, teda pri reakciách vždy sledoval konštantný objemový pomer, tento vedec dospel k nasledujúcemu zákonu reakcií v plynných objemoch, známemu ako Objemové právo Gay-Lussac alebo Zákon kombinácie zväzkov:

Vyhlásenie o volumetrickom zákone Gay-Lussaca
Ale tento zákon bol proti Daltonova atómová teória, ktorý hovoril, že všetko bolo tvorené masívnymi a nedeliteľnými sférickými časticami, atómami. Podľa tejto teórie by sa objem produktov v reakcii mal rovnať súčtu objemov reaktantov. Malo by sa tak stať:
Vodík + kyslík → voda
2 zväzky + 1 zväzok → 3 zväzky
Gay-Lussac ale ukázal, že to tak v praxi nebolo, výsledok sa rovnal dvom objemom vodnej pary.
Teraz neprestávajte... Po reklame je toho viac;)
Odpoveď na tento zjavný rozpor prišla hypotéza alebo Avogadrov zákon.

Pečiatka vytlačená v Taliansku ukazuje Amedea Avogadra a vypovedanie jeho zákona v roku 1956 *
Amedeo Avogadro (1776-1856) ukázali, že v skutočnosti plyny neboli izolované atómy, ale molekuly (s výnimkou vzácne plyny). Jeho zákon hovoril:

Vyhlásenie zákona Avogadro
Avogadro to ukázal 1 mól akéhokoľvek plynu má 6,02. 1023 molekuly. Táto hodnota je známa ako Avogadrovo číslo alebo konštanta. Bolo dokázané, že za normálnych podmienok teploty a tlaku (CNTP), v ktorých je tlak rovný 1 atm a teplota je 273 K (0 ° C), objem obsadený 1 mólom plynu bude vždy 22,4 l. Táto hodnota zodpovedá molárny objem plynov. Tieto vzťahy sú veľmi dôležité pre riešenie cvičení stechiometria.
Môže sa to zdať čudné, pretože môže vzniknúť nasledujúca otázka: Ako by mohli plyny s molekulami a atómami rôznych veľkostí zaberať rovnaký objem?
Je to tak preto, lebo molekuly plynu sú tak vzdialené od seba, že veľkosť molekúl je zanedbateľná.
Týmto spôsobom Avogadrov volumetrický zákon vysvetľoval volumetrický zákon Gay-Lussaca. Ďalej si všimnite, že dve molekuly vodíka (dva objemy) reagujú s jednou molekulou kyslíka (jeden objem) za vzniku dvoch molekúl vody (dva objemy). Voda a vodík majú rovnaký objem, pretože majú rovnaké množstvo molekúl, ako uvádza Avogadrov zákon.
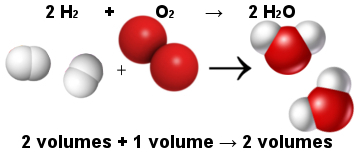
Podiel medzi molekulami v reakcii formovania vody
Avogadrov zákon súčasne ustálil atómovú teóriu, pretože vidíte, že v reaktantoch aj v produktoch je celkovo 6 atómov (4 vodík a 2 kyslík).
Tieto volumetrické zákony boli veľmi dôležité pre vývoj koncepcie molekuly.
* Obrázok chránený autorskými právami: veža76 / Shutterstock.com
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Objemový zákon Gay-Lussaca“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/lei-volumetrica-gay-lussac.htm. Prístup k 28. júnu 2021.
Čo sú plyny, aké sú vlastnosti plynov, molekulárne zlúčeniny, stlačiteľnosť, stály objem, kinetická energia priemerná absolútna teplota plynu, ideálny plyn, skutočné plyny, dokonalý plyn, premenné stavu plynu, objem plynu, ročné obdobia
Chémia

Zákony Gay-Lussac, Proustov zákon, chemická reakcia, konštantný pomer, množstvo látok, čistá látka, analýza kvalitatívny a kvantitatívny, zákon dokonalých plynov, zákon konštantných rozmerov, zákon určitých pomerov, zákon volumetrický.