Ako je uvedené v textoch „Elektromagnetické spektrum chemických prvkov„a“Emisné a absorpčné spektrum a Kirchhoffove zákony”, Diskontinuálne emisné spektrá každého chemického prvku sú odlišné.

Nižšie teda máme zreteľné spektrum niektorých z týchto prvkov:

Dánsky fyzik Niels Böhr (1885-1962) si teda uvedomil, že to môže súvisieť so štruktúrou atómu každého z týchto prvkov. Navrhol teda atómový model, ktorý doplnil Rutherfordov model, ale zameral sa na správanie okolitých elektrónov v jadre atómu.
Pred časom Max Planck (1858-1947) navrhol teóriu, že elektróny sú vyčíslený, v tom zmysle, že emitovať a absorbovať konkrétne množstvo energie, akoby to boli malé balíčky energie, ktorú nazval koľko (kvantová, v jednotnom čísle).
Böhr teda navrhol toto: keďže každý prvok má iné spektrum, má každý prvok vo svojom atóme elektróny konštantnej a rozdielnej energie od prvku k prvku.
Každý elektrón môže zostať iba na určitej konkrétnej obežnej dráhe, pretože na každej z týchto dráh má elektrón konštantnú, dobre definovanú a charakteristickú energiu. Elektrón môže obsadzovať iba energetické úrovne, pre ktoré má príslušnú energiu.
Teraz neprestávajte... Po reklame je toho viac;)
Spektrá sú nespojité, pretože elektróny sú kvantované.
Elektrón môže meniť hladiny iba vtedy, ak absorbuje energiu. Napríklad keď spaľujete sodnú soľ v Bunsenovom horáku, dodávate energiu elektrónom. Pri absorpcii kvanta energie elektrón preskočí na inú energetickejšiu hladinu a zostane v excitovanom stave. Základný stav je však stabilnejší, takže tento elektrón emituje absorbovanú energiu a vracia sa na svoju pôvodnú obežnú dráhu. Vydáva túto energiu vo forme elektromagnetických vĺn, ktoré je možné vizualizovať vo forme svetla. V prípade sodíka má toto svetlo intenzívne žltú farbu. Keď teda tieto vlny prechádzajú cez hranol, získa sa diskontinuálne spektrum sodíka.
Takže pre Böhru, každá svetelná čiara, ktorá sa objavila v diskontinuálnom spektre prvkov, naznačovala energiu uvoľnenú pri návrate elektrónu z jednej vonkajšej úrovne na druhú bližšie k jadru.
Obrázok nižšie pomáha lepšie pochopiť tento problém:
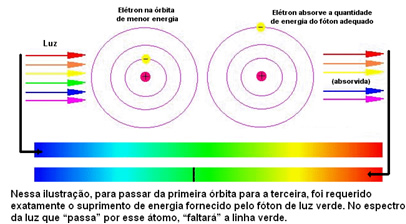
Pretože atómy každého prvku majú povolené iba určité energetické hodnoty, ktoré zodpovedajú energetickým vrstvám, pre každý prvok existuje iné spektrum.
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. „Štruktúra elektromagnetického spektra a atómu“; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/espectros-eletromagneticos-estrutura-atomo.htm. Prístup k 27. júnu 2021.