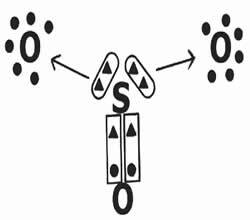
Organokovový sú organické zlúčeniny, ktoré majú najmenej jeden atóm kovu naviazaný na atóm uhlíka. Kovy, ktoré tvoria tento typ látky, sú zvyčajne: horčík (Mg), zinok (Zn), olovo (Pb) a ortuť (Hg).
Medzi najbežnejšie organokovové látky patrí organomagnézium, známejšie ako Grignardove zlúčeniny alebo činidlá, ktorého kovom viazaným na uhlík je horčík, a ten je zase viazaný na halogén, ktorým môže byť jeden z nasledujúcich prvkov rodiny 17 periodickej tabuľky: fluór (F), chlór (Cl), bróm (Br) a jód (I).
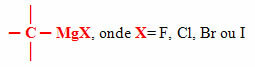
Organokovové zlúčeniny sú zvyčajne toxické, pretože obsahujú kovy, ktoré sa hromadia v tele a sú rozpustnejšie v organických zlúčeninách ako iné anorganické zlúčeniny, ktoré ich obsahujú kovy. Príkladom toho je, keď baníci alebo priemyselné podniky vrhajú organokovové zlúčeniny do jazier a riek. Výsledkom sú vážne problémy pre zdravie používateľov týchto vôd (ľudí aj zvierat), ako aj ďalšie ekologické problémy.
Ďalej uvádzame tri príklady organokovových zlúčenín prítomných v našom každodennom živote:
• Etylchlorid ortuťnatý (H3C CH2 ─ HgCl): táto zlúčenina sa môže použiť ako fungicíd pri konzervácii semien. Jeho použitie je však veľmi nebezpečné, pretože obsahuje ortuť, a je vysoko toxický, najmä pre nervový systém;
• Butyllítium (H3C CH2 ─ CH2 ─ CH2 ─ Li): táto zlúčenina sa používa ako iniciátor polymerizácie na výrobu elastomérov, to znamená polymérov s elastickými vlastnosťami;
• Tetraetyl-olovo (alebo tetraetyl-olovo): táto zlúčenina sa dlho používala ako antiblokovací prostriedok proti benzínu, pretože zvyšovala jej oktánové číslo a účinnosť motora. Spolu so spaľovaním benzínu však táto uvoľnená zlúčenina viedla do životného prostredia a spôsobovala znečistenie ovzdušia. Toto olovo je toxické, znečisťuje životné prostredie a je obzvlášť nebezpečné, pretože ovplyvňuje mozog a má vplyv na motorickú koordináciu.
Teraz neprestávajte... Po reklame je toho viac;)
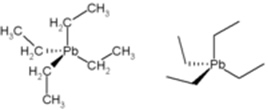
Štruktúra tetraetyl-olova.
Na jeho miesto sa teda používa iný organokov: ferocén, ktorý má vo svojej štruktúre dva cyklopentadienylové kruhy na každej strane železa, ako je znázornené v chemických štruktúrach nižšie:
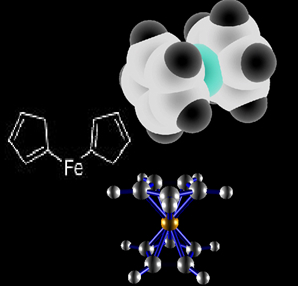
Štruktúra ferocénu.
Nomenklatúra organometaliky sa riadi nasledujúcou schémou:

Príklady:
CH3
│
CH2
│
H3C ─ CH2 ─Al: trietylalumínium
│
CH2
│
CH3
H3C ─ CH2 ─ CH2 ─ Li: propyllithium
Ak ide o Grignardovu zlúčeninu, máme:

Príklady:
H3C CH2 ─ MgCl: etylchlorid horečnatý
H2C ═ CH ─ MgBr: vinylbromid horečnatý
Autor: Jennifer Fogaça
Vyštudoval chémiu
Prajete si odkaz na tento text v školskej alebo akademickej práci? Pozri:
FOGAÇA, Jennifer Rocha Vargas. "Organokovové zlúčeniny"; Brazílska škola. Dostupné v: https://brasilescola.uol.com.br/quimica/compostos-organometalicos.htm. Prístup k 27. júnu 2021.