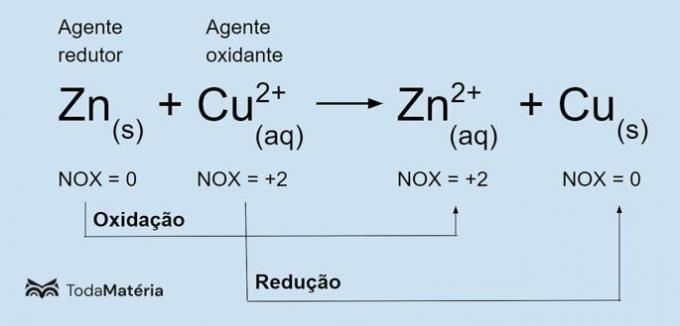
Электронное распределение электронов атома в нейтральном или основном состоянии обычно выполняется с помощью Диаграмма Полинга, показано ниже:
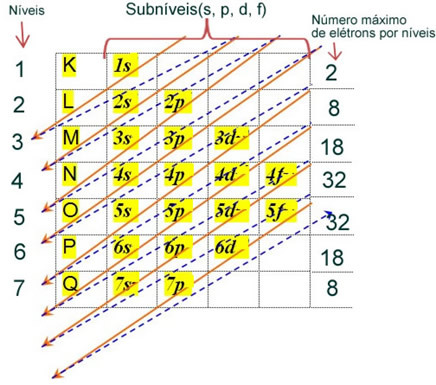
Подробные правила этого распространения можно найти в следующих двух текстах на нашем веб-сайте: «Электронное распределение электронов" а также "Правила электронного распространения”.
Электронное распределение ионов изначально работает так же, как и для атомов в нейтральном состоянии; только с одним отличием. Поскольку ион - это атом, который приобрел или потерял электроны, мы должны это учитывать и сделать следующее:

Важное наблюдение: изменение происходит на самом внешнем подуровне и не на самом энергичном.
если ион катион, мы должны удалить электроны что он проиграл. Давайте посмотрим на пример:
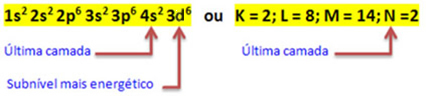
Атом железа (атомный номер = 26) имеет следующее электронное распределение по подуровням в энергетическом порядке: 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d6. Что касается электронных слоев, то у нас есть: K =2; L = 8; М = 14; N = 2.
Это распределение показано на диаграмме Полинга ниже:
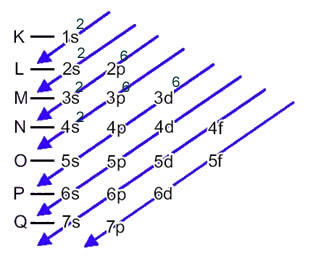
Когда атом железа теряет 2 электрона, он превращается в катион Fe.2+. Итак, при создании вашей электронной рассылки мы должны удалить 2 электрона из последней оболочки(N) и не самый энергичный подуровень, как показано ниже:
Не останавливайся сейчас... После рекламы есть еще кое-что;)
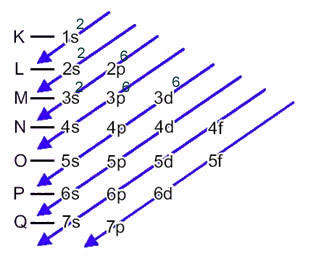
Таким образом, электронное распределение катиона Fe2+ дан кем-то:
1 с2 2 с2 2p6 3 с2 3p6 3d6 или же К = 2; L = 8; M = 14
Теперь, если нам нужно выполнить электронную раздачу анион, мы должны сложить полученные электроны.Посмотрите, как это делается, в следующем примере:
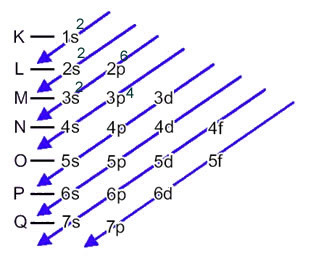
Анион серы (16s2-) образуется из атома серы (16S) за счет усиления 2 электронов, на что указывает заряд 2-. Его электронное распределение в основном состоянии определяется выражением:
1 с2 2 с2 2p6 3 с2 3p4 или же К = 2; L = 8; M = 6
В этом случае последний подуровень совпадает с подуровнем энергии 3p. Итак, мы добавляем к нему два электрона аниона серы:
1 с2 2 с2 2p6 3 с2 3p6 или же К = 2; L = 8; M = 8
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Электронное ионное распределение»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm. Доступ 27 июня 2021 г.