НАШИ общая концентрация, также называемая концентрацией в г/л, представляет собой отношение массы растворенного вещества к объему раствора.
Математически общая концентрация выражается формулой:
С = м/об
Где,
C: обычная концентрация;
m: масса растворенного вещества;
V: объем раствора.
Наиболее часто используемой единицей измерения концентрации является г/л, так как масса растворенного вещества рассчитывается в граммах (г), а объем раствора в литрах (л).
Например, морская вода имеет большое количество растворенных солей, и хлорид натрия (NaCl), широко известный как поваренная соль, является одной из них.
Концентрация хлорида натрия в морской воде в среднем составляет 2,5 г/л. Итак, в 1 литре морской воды, которая является раствором, содержится 2,5 грамма соли, которая является растворенным веществом.
Как рассчитать общую концентрацию?
Раствор – это однородная смесь, образованная меньшим количеством вещества, называемого растворенным веществом, растворенным в растворителе, находящемся в большем количестве.
Следовательно, общая концентрация относится к количеству растворенного вещества в данном объеме раствора. Чем больше растворенного вещества растворено в растворе, тем он более концентрированный. В противном случае, то есть низкое содержание растворенного вещества, указывает на то, что раствор разбавлен.
Пример 1: Какова концентрация в г/л раствора йодида серебра (AgI), содержащего 2,6 г в 1 л раствора?
Получив количество растворенного вещества и объем раствора, мы просто подставляем значения в общую формулу концентрации, чтобы найти его значение.
Следовательно, в растворе йодистого серебра с концентрацией 2,6 г/л на каждый 1 л раствора приходится 2,6 г растворенного вещества.
Пример 2: При выпаривании растворителя из 500 мл физиологического раствора с концентрацией 6 г/л какая масса растворенного вещества получается?
Обратите внимание, что в некоторых расчетах мы можем найти общую описанную концентрацию, чтобы мы могли рассчитать массу растворенного вещества.
Также необходимо обратить внимание на агрегаты. Поскольку обычная концентрация выражается в г/л, в этом случае нам необходимо преобразовать единицу объема перед применением формулы.
Так как в 1 л содержится 1000 мл, то 500 мл соответствует 0,5 л.
Так, при выпаривании растворителя из раствора с концентрацией 6 г/л было получено 12 г растворенного вещества.
Получите больше знаний с содержанием:
- Концентрация раствора
- молярная концентрация
- Разведение растворов
Решенные общие упражнения на концентрацию
Используйте следующие вопросы, чтобы проверить знания, полученные ранее.
Вопрос 1
(Unicamp) Растворитель полностью выпаривают из 250 мл водного раствора MgCl.2 концентрации 8,0 г/л. Сколько граммов растворенного вещества получилось?
а) 8,0
б) 6,0
в) 4,0
г) 2,0
д) 1,0
Правильный вариант: г) 2.0.
вопрос 2
См. изображение ниже.
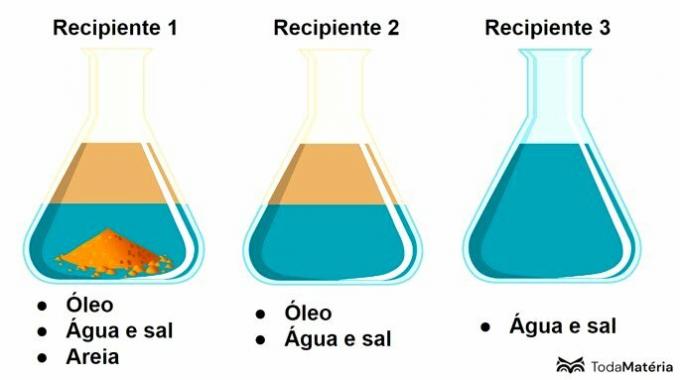
В этой схеме контейнер 3 содержит
а) гетерогенная смесь
б) чистое вещество
в) Решение
г) коллоидная смесь
Правильный вариант: в) Решение.
Контейнер 3 содержит раствор, представляющий собой гомогенную смесь, образованную растворенным веществом и растворителем, где соль является растворенным веществом, а вода - растворителем.
В целом можно сказать, что растворенное вещество является компонентом в наименьшем количестве, а растворитель присутствует в наибольшем количестве.
Контейнер 1 представляет собой гетерогенную смесь из 3 фаз, а контейнер 2 соответствует гетерогенной смеси из 2 фаз.
вопрос 3
Раствор готовят растворением 4,0 г хлорида магния MgCl.2 до достижения концентрации 2,0 г/л. Какой объем раствора приготовили?
а) 1 л
б) 2 л
в) 4 л
г) 6 л
Правильный вариант: б) 2 л.
Ознакомьтесь с дополнительными проблемами с комментариями по адресу обычные упражнения на концентрацию.
Библиографические ссылки
ФОНСЕКА, М. Р. М. Химия, 1. 1. изд. Сан-Паулу: Аттика, 2013.
САНТОС, WLP; МОЛ, Г.С. Гражданская химия, 1. 2. изд. Сан-Паулу: Editora AJS, 2013.
УБЕРКО, Дж. Подключить химию, 1. 2. изд. Сан-Паулу: Сарайва, 2014.
- Упражнения на общую концентрацию с комментариями
- химические растворы
- Солют и растворитель: что это такое, отличия и примеры
- Концентрация раствора
- Растворимость
- Молярность или молярная концентрация: что это такое, формула и как рассчитать
- Разведение растворов
- Упражнения по свойствам материи