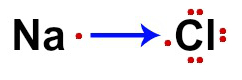
THE молекулярная геометрия, то есть расположение атомов в молекуле, можно определить по правилу химика Гиллеспи, в котором он перечисляет количество атомов, присоединенных к центральному атому, и количество облаков. электроника.
Знания о геометрии молекулы чрезвычайно важны, потому что они помогают нам определяют полярность и, как следствие, растворимость (по правилу аналога растворяет похожий).
с звонком тетраэдрическая геометрия, ничем не отличается. Смотрите критерии его определения по правилам Гиллеспи:
Пятиатомные молекулы (пять атомов);
Отсутствие электронных облаков в центральном атоме;
составные молекулы или составные анионы.
Некоторый примеры молекул с тетраэдрической геометрией они есть:
CH4

Структурная формула CH4
Углерод имеет четыре электрона в валентной оболочке, и все эти электроны связаны с атомами водорода. Вот почему у углерода нет электронного облака (лишней пары электронов).
ТОЛЬКО4-2
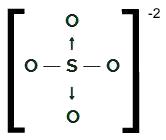
Структурная формула ОС4-2
Сера, имеющая шесть электронов в валентной оболочке, образует две одинарные связи с двумя атомами кислорода и двумя
дативные ковалентные связи с двумя другими атомами кислорода. В одинарных связях он использует два своих электрона и в каждом дательном падеже он использует еще два (всего четыре электрона, участвующих в дательном падеже), всего шесть электронов. Таким образом, на нем не осталось облаков.NH4+

Структурная формула NH4+
Азот, который имеет пять электронов в валентной оболочке, образует три одинарные связи с атомами водорода и дативную связь с другим водородом. В одинарных связях он использует три своих электрона, а в дательном падеже - еще два, всего пять электронов. Таким образом, на нем не осталось облаков.
CH3Cl
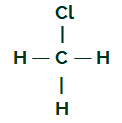
Структурная формула CH3Cl
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Углерод имеет четыре электрона в валентной оболочке, и все эти электроны связаны с атомами водорода и атомом хлора. По этой причине у углерода нет электронного облака.
→ Полярность молекул
Зная, что данная молекула имеет тетраэдрическую геометрию, мы можем определить ее полярность чрезвычайно простая форма, так как у молекулы заняты четыре полюса (четыре лиганда в атоме центральный). Для этого достаточно знать характеристики связующих и учитывать одно из следующих правил:
Если количество облаков равно количеству равных лигандов = неполярная молекула;
Если количество облаков отличается от количества равных лигандов = полярная молекула.
В следующих двух молекулах, геометрия которых является тетраэдрической, мы можем применить приведенные выше правила и указать их полярность:
Молекула метана
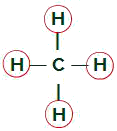
Равные лиганды в молекуле метана
Молекула метана имеет четыре электронных облака (четыре одинарные связи), а также четыре атома водорода, прикрепленных к центральному атому. Таким образом, у нас естьчетыреоблака и четыре одинаковых связующих, скоро, молекула неполярна.
Наблюдение: Если молекула вещества аполат он хорошо растворяется в другом веществе, молекулы которого также неполярный.
Молекула хлорметана

Равные лиганды в молекуле хлорметана
Молекула хлорметана имеет четыре электронных облака (четыре одинарные связи) и три атома водорода и один атом хлора, присоединенных к центральному атому. Таким образом, у нас естьчетыреоблака и три равных лиганда (три атома водорода); скоро молекула полярна.
Наблюдение: Если молекула вещества полярный он хорошо растворяется в другом веществе, молекулы которого также полярный.
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Тетраэдральная геометрия»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/geometria-tetraedrica.htm. Доступ 28 июня 2021 г.