В химические формулы представляют собой представления, используемые для обозначения химических элементов, входящих в состав вещества, а также для представления типа взаимодействия между участвующими атомами.
Через анализ формула химического вещества, мы можем определить природу химических связей (ионный, ковалентный или металлический), который его сформировал, а также его физико-химическое поведение. Некоторые из свойств, связанных с физико-химическим поведением вещества:
Растворимость
Точка слияния
Точка кипения
Реактивность
Теперь узнайте типы соединений, из которых состоят химические вещества, а также формулы, которые их представляют.
Типы соединений
) ионные соединения
Ионные соединения - это все химические вещества, образованные ионной связью между атомами, то есть в этих соединениях есть атомы, которые теряют, и атомы, которые получают электроны. Комбинация химических элементов, образующих этот тип соединения, может быть:
Металл с металлом
Металл с водородом
б) Ковалентные соединения
Ковалентные соединения - это все химические вещества, образованные ковалентной связью между атомами, то есть в этих соединениях есть атомы, которые обмениваются электронами друг с другом. Комбинация химических элементов, образующих этот тип соединения, может быть:
металл в металл
Аметалл с водородом
водород с водородом
в) Соединения металлов
Металлические соединения - это все химические вещества, образованные атомами одного металлического элемента. В этих соединениях атомы обмениваются электронами только друг с другом.
Формулы ионных соединений
) ионная формула
Формула ion указывает количество атомов, которые образуют ионную единицу соединения, как в случае хлорида. натрия, формула которого - NaCl. В формуле мы отождествляем наличие атома натрия и атома хлор.
Чтобы построить ионную формулу, просто скрестите заряды каждого из ионов, составляющих ионное соединение. Для катиона Al+3 и анион O-2, например, когда мы пересекаем заряды и не обращаем внимания на сигналы, мы получаем следующую формулу ion:
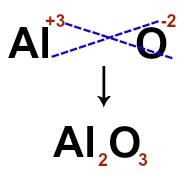
б) Электронная формула
Электронная формула используется для представления потерь и усиления электронов атомов, участвующих в образовании соединения. Вокруг аббревиатуры каждого элемента у нас есть каждый из электронов валентные слои.
В случае хлорида натрия (NaCl) в Na представлен только один валентный электрон (потому что он принадлежит к семейству IA), а в Cl - семь валентных электронов (поскольку он принадлежит к семейству VIIA).
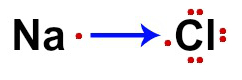
Электронная формула NaCl
Усиление электрона Cl (неметаллом) и потеря электрона Na (неметаллом) показано стрелкой. Согласно теория октетов, Na теряет электрон из-за того, что имеет только один, а Cl получает один, чтобы заполнить восемь валентных электронов.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Для ковалентных соединений
а) Молекулярная формула
Молекулярная формула используется для обозначения в упрощенной форме ковалентного вещества. Молекулярная формула воды - H2O, например, имеет два атома водорода и один атом кислорода.
В отличие от ионной формулы ионных соединений, молекулярная формула ковалентного соединения не построена так простота, поскольку разное количество атомов одних и тех же элементов образуют разные вещества, такие как вода (ЧАС2O) и перекись водорода (H2О2).
В упражнениях очень часто встречается молекулярная формула:
Обеспечиваться самим упражнением;
Определяться расчетом;
Определяться путем подсчета каждого элемента по структурной формуле;
Определяться по названию вещества.
б) Структурная формула
Структурная формула ковалентного вещества используется для обозначения количества связей, которые каждый из атомов создает в молекуле. В структурной формуле используются следующие ссылки:
Одиночная ссылка: обозначена дефисом (─), обозначает одиночную ссылку;
Двойная связь: представлена двумя черточками (=), обозначает две связи;
Тройная связь: представлена тремя штрихами (≡), обозначает три связи;
дательная ссылка: представлен стрелкой (→), указывает на одно соединение.
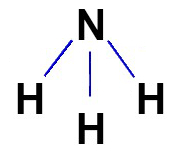
Структурная формула ковалентных соединений должна быть представлена, когда это возможно, в соответствии с молекулярной геометрией рассматриваемой молекулы. См. Представление структурной формулы аммиака, имеющей пирамидальную геометрию:
в) Электронная формула
Электронная формула ковалентного соединения демонстрирует распределение электронов между атомами, составляющими молекулу. Вместо штрихов, используемых в структурной формуле, мы используем сферы для обозначения электронов, разделяемых между атомами. Посмотрите:
Одинарная связь: разделение двух электронов (по одному от каждого из задействованных атомов);
Двойная связь: четыре электрона (по два от каждого из участвующих атомов);
Тройная связь: разделение шести электронов (по три от каждого из задействованных атомов);
Дативная связь: разделение двух электронов (оба из одного атома между участниками),
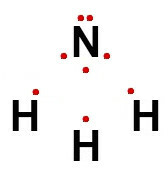
Таким образом, для аммиака, структурная формула которого была представлена выше, его электронная формула:
Для металлических соединений
Соединения металлов, поскольку они образованы исключительно из атомов одного металла, имеют в качестве своей химической формулы сокращение химического элемента:
Медное вещество: Cu
Золотое вещество: Au
Вещество железа: Fe
Автор: Диого Лопес Диас
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Формулы химических веществ»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/formulas-substancias-quimicas.htm. Доступ 27 июня 2021 г.