Căldurălatent este suma de energietermic care este absorbit sau renunțat de un corp sau de un sistem termodinamic, în timpul unei modificări a stării sale fizice, în temperatura constantă.
Când o substanță pură atinge temperatura sa de Fuziune sau fierbere, în timpul încălzirii, starea fizică începe să se schimbe. În acest proces, continuă să absoarbă căldura, totuși temperaturarămâneconstant. Acest lucru se întâmplă deoarece, la atingerea acestor temperaturi, în care apar modificări ale stării fizice, toată căldura care este absorbită de sistemul termodinamic este utilizată pentru a depăși energiepotenţial care își păstrează moleculele laolaltă. De îndată ce sistemul termodinamic absoarbe toată energia necesară ruperii moleculelor sale, interacțiunea dintre ele scade, indicând faptul că starea lor de agregare s-a schimbat. După schimbarea stării fizice, căldura care a fost absorbită izoterm continuă să fie absorbită de molecule, asigurându-le energiecinetica. Acest tip de căldură care crește energia cinetică a moleculelor se numește căldură sensibilă.
Uitede asemenea: Șapte sfaturi „aur” pentru un studiu de fizică mai eficient
O căldurălatent măsoară cantitatea de căldură, pe unitate de masă, necesară pentru orice schimbare starea fizică a corpului, prin urmare, unitatea sa de măsură, conform Sistemului Internațional (SI), este Joulepekilogram (J / kg). Cu toate acestea, utilizarea altor unități, cum ar fi caloriepegram (cal / g), este destul de frecvent în studiul calorimetriei.
Tipuri de căldură latentă
Există două tipuri de căldură: o căldurădacănivel este căldurălatent. Căldura sensibilă este cea care este transferată între corpuri atunci când există schimbări de temperatură. La rândul său, căldura latentă apare atunci când există transferuri de căldură fără modificări de temperatură.
Căldura latentă este modificată pentru diferite modificări ale stării fizice. Verificați diferitele tipuri de căldură latentă:
căldură latentăînfuziune (LF): este căldura care este absorbită sau renunțată de corpuri în timpul procesului de fuziune: de la lichid la solid și invers, cu temperatură constantă.
căldură latentăînvaporizare (LV): este cel care este transferat în timpul transformărilor solid-lichid sau lichid-solid, în temperatura constantă.
Uitede asemenea: Ce este capacitatea termică?
Exempleîncăldurălatent
Consultați câteva situații de zi cu zi în care există schimburi de căldură latente:
Când încălzim apa, până la o temperatură de 100 ° C, începe procesul de evaporare. Atâta timp cât toată apa nu se transformă în vapori, temperatura acesteia nu se schimbă.
Când turnăm apă pe o suprafață foarte fierbinte, toată apa se vaporizează aproape instantaneu. Acest proces se numește încălzire și implică absorbția căldurii latente.
Există un schimb de căldură latent atunci când atingem o sticlă de sodă la temperaturi scăzute și tot conținutul acesteia îngheață rapid la o temperatură constantă, datorită temperaturii sale mai mici decât punctul de topire al apei.
formula de căldură latentă
Căldura latentă este calculată prin raportul dintre cantitatea de căldură transferată în transformarea izotermă:
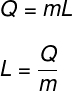
Î - cantitatea de căldură transferată
m - masa corpului
L - căldură latentă
Schimbări de fază și căldură latentă
Se produc modificări de fază în substanțele pure întemperaturaconstant, prin absorbția sau eliberarea căldurii latente. Toate substanțele pure au o curba de încălzire similar cu imaginea de mai jos:
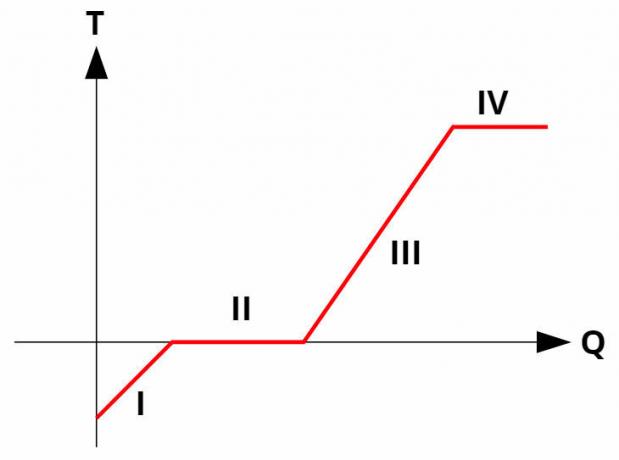
La curbeînIncalzi ele raportează temperatura (axa y) la cantitatea de căldură dată sau primită (axa x). În schimbările de fază (procesele II și IV), temperatura rămâne constantă, deși există încă schimb de căldură.
Vezi și: Bazele calorimetriei
masă de căldură latentă
În condiții normale de temperatura și presiune, O căldurălatent de apă, pentru diferitele sale modificări ale stării fizice, este prezentat în tabelul de mai jos:
Transformare |
Căldură latentă (cal / g) |
Fuziune (0 ° C) |
80 |
Solidificare (0 ° C) |
-80 |
Vaporizare (100 ° C) |
540 |
Condensare (100 ° C) |
-540 |
Conform tabelului prezentat mai sus, 80calorii a ingheta 1 gramde apă la temperatura de topire (0 ° C). Semnele negative din procese de solidificare și condensare indicați că s-a eliberat căldură în ele, deci aceste două transformări sunt exoterm. Tabelul de mai jos arată căldura latentă din J / kg, pentru aceleași procese:
Transformare |
Căldură latentă (J / kg) |
Fuziune (0 ° C) |
333.103 |
Solidificare (0 ° C) |
-333.103 |
Vaporizare (100 ° C) |
2,2.106 |
Condensare (100 ° C) |
-2,2.106 |

exerciții de căldură latentă
1) Un recipient conține 500 g de apă lichidă. Fără modificări ale temperaturii apei, tot conținutul său este evaporat brusc. Determinați cantitatea de căldură transferată în conținutul acestui recipient.
Date: LF = 540 cal / g
Rezoluţie:
Pentru a calcula cantitatea de căldură necesară pentru evaporarea acestei mase de apă, vom folosi următoarea formulă:
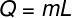
Folosind datele furnizate de exercițiu, vom face următorul calcul:
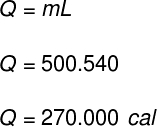
De mine. Rafael Helerbrock
