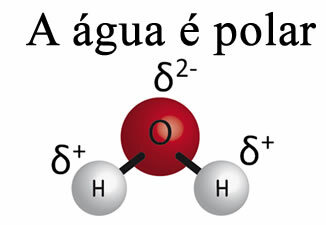
Apa singură nu poate îndepărta grăsimea din materiale. Asta pentru ca apa este polară, așa cum se arată în imaginea de mai jos, din cauza diferenței de electronegativitate care există între atomii de hidrogen și oxigen ai moleculelor lor. Pe de altă parte, grăsimea este nepolară și, prin urmare, apa nu dizolvă grăsimile.
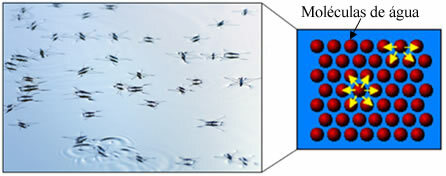
În plus, apa are ceva numit tensiune superficială. Puteți înțelege acest lucru mai bine în text. Tensiunea superficială a apei, dar practic este un fel de film elastic sau membrană care se formează la suprafața apei, care îl împiedică să pătrundă în țesături și alte materiale pentru a îndepărta murdăria. Moleculele de apă se atrag reciproc în toate direcțiile legături de hidrogen, dar moleculele de suprafață interacționează doar cu moleculele laterale și inferioare, creând o diferență în forțe de coeziune, ceea ce face ca moleculele de suprafață să se contracte și să formeze această tensiune superficială.
Aici intră săpunurile și detergenții (din latină detoxifiază = clar), care se mai numesc
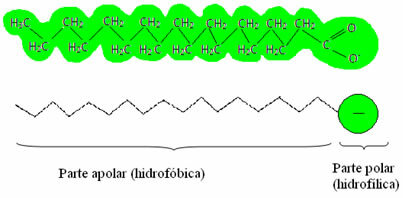
agenți activi de suprafață, deoarece au capacitatea de a reduce tensiunea superficială a apei și, în plus, interacționează atât cu apa, cât și cu grăsimea. Cum se întâmplă acest lucru?Săpunurile și detergenții au săruri de acizi grași, care sunt molecule lungi formate de o parte nepolare (ce este hidrofob – hidro = apă; fobi = aversiune) și a capăt polar (hidrofil – hidro = apă; filă = prieten). Mai jos avem o structură tipică a săpunului:
În general, detergenții sunt săruri ale acizilor sulfonici cu lanț lung:
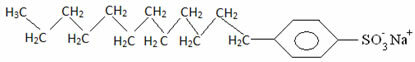
Astfel, partea nepolare a acestor molecule prezente în săpunuri și detergenți interacționează cu grăsimea, în timp ce capătul polar interacționează cu apa, grupându-se în globule mici, chemat de la micele, în care părțile hidrofile se confruntă cu exteriorul micelei în contact cu moleculele de apă și grăsimea rămâne în interior, în contact cu partea nepolară sau hidrofobă, un proces similar cu cel prezentat în imagine a urma:
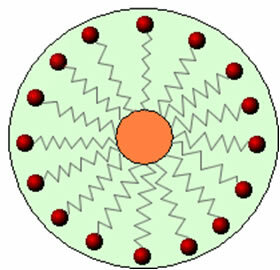
În acest fel, murdăria grasă este prinsă în centrul micelelor și poate fi îndepărtată. Un alt punct este că detergenții și săpunurile au capacitatea de a reduce tensiunea superficială a apei, deoarece reduce interacțiunile dintre moleculele sale, facilitând astfel pătrunderea în diverse materiale pentru a îndepărta murdărie.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm