Învață să aplici prima lege a termodinamicii în diferite situații, rezolvă exerciții și testează-ți cunoștințele cu exerciții rezolvate și explicate.
intrebarea 1
Prima lege a termodinamicii spune ca:
a) Energia nu poate fi creată sau distrusă, dar poate fi convertită dintr-o formă în alta.
b) Energia este întotdeauna conservată, dar nu poate fi convertită dintr-o formă în alta.
c) Energia poate fi creată sau distrusă, dar nu poate fi convertită dintr-o formă în alta.
d) Energia nu poate fi conservată, dar poate fi convertită dintr-o formă în alta.
Prima lege a termodinamicii este principiul conservării energiei, deci într-un sistem închis, cantitatea de energie rămâne constantă și nu poate fi transformată decât dintr-o formă în alta. alte.
intrebarea 2
Să presupunem un sistem închis care primește 100 J de căldură în timp ce lucrează 50 J. Care este modificarea energiei interne a sistemului?
a) -50J
b) 0 J
c) 50J
d) 100J
e) 150J
Verificarea semnelor:
Căldura primită este Q pozitivă > 0.
Lucrul efectuat este pozitiv W > 0.
Conform primei legi, avem:
intrebarea 3
Un sistem de gaz ideal schimbă 500 de jouli de căldură cu mediul extern. Presupunând că acest proces este o răcire izometrică, determinați lucrul și respectiv energia internă.
a) 500 J și 0 J
b) - 500 și 0 J
c) 0 J și 500 J
d) 0 J și - 500 J
e) -500 J și 500 J
Deoarece procesul este izometric, nu există nicio modificare a volumului, deci munca este zero.
Conform primei legi a termodinamicii:
Deoarece este o răcire, sistemul pierde căldură, prin urmare:
intrebarea 4
8 moli de gaz ideal într-un sistem piston-cilindru sunt comprimați efectuând 1000 J de lucru. În timpul procesului, 400 J de căldură sunt pierdute în mediul extern. Energia sa internă și, respectiv, modificarea temperaturii sale sunt egale cu
Dat: R = 8,31 J/mol. K
a) - 1400 J și variație aproximativă de 6 K
b) 600 J și variație aproximativă de 6 K
c) 600 J și variație aproximativă de 14 K
d) - 1400 J și variație aproximativă de 14 K
energie interna
Pe măsură ce sistemul primește lucru, semnul său este negativ, la fel și căldura, care în acest proces se pierde.
Prima lege a termodinamicii este:
Înlocuind valorile, obținem:
R = 8,31 J/mol K
Temperatura
Prin legea lui Joule avem:
intrebarea 5
Un gaz perfect suferă compresie, făcând 500 J de lucru. La sfârșitul acestei transformări, energia internă a sistemului s-a schimbat cu 200 J mai puțin decât la început. Cantitatea de căldură schimbată de gaz a fost
a) - 700 J
b) - 300 J
c) 300J
d) 0J
e) 700 J
Din moment ce lucrarea a fost primită, adică lucrarea rezistentă, semnul ei este negativ.
Înlocuirea valorilor în ecuația primei legi a termodinamicii:
intrebarea 6
(CEDERJ 2021) Intr-o etapa a ciclului executata de un gaz ideal intr-un aparat de aer conditionat, presiunea gazului este crescuta pastrandu-i volumul constant. În această etapă a ciclului, munca W efectuată de gaz, cantitatea de căldură Q absorbită de acesta și modificarea ΔT a temperaturii acestuia sunt, respectiv:
a) W < 0, Q < 0 și ΔT < 0
b) W = 0, Q > 0 și ΔT > 0
c) W = 0, Q = 0 și ΔT = 0
d) W > 0, Q > 0 și ΔT > 0
Date:
Presiunea P crește;
Volumul rămâne constant;
Muncă
Deoarece volumul este constant, lucrul W este egal cu zero.
Prima lege a termodinamicii merge astfel:
Deoarece căldura este pozitivă, modificarea energiei interne va fi de asemenea pozitivă.
Căldură
Deoarece căldura este absorbită, este pozitivă.
Temperatura
Conform legii gazelor:
Unde,
n este numărul de moli
R este constanta universală a gazului
Astfel, temperatura depinde doar de presiune, deoarece volumul este constant, fiind pozitiv.
intrebarea 7
(UNICENTRO 2018) Conform primei legi a termodinamicii, modificarea energiei interne a unui sistem, ΔU, este dat de diferența dintre căldura schimbată cu mediul exterior, Q, și munca, W, efectuată în proces termodinamic. Având în vedere aceste informații, dacă un gaz monoatomic se extinde astfel încât să rămână mereu la aceeași temperatură, această transformare poate fi reprezentată prin ecuația
a) ΔU + W = 0
b) ΔU − W =0
c) Q − W = 0
d) Q + ΔU = 0
Procesul izoterm are loc fără schimbarea temperaturii.
Energia este legată de temperatură prin:
Unde n este numărul de moli și R este constanta universală a gazului. Deoarece n și R sunt constante, există doar variație de temperatură și
Prima lege a termodinamicii merge astfel:
intrebarea 8
(URCA 2016) Conform primei legi a termodinamicii dacă, în timpul unui proces izoterm suferit de un gaz ideal de masă fixă, gazul eliberează o cantitate de căldură a cărei magnitudine este de 50 cal, atunci modificarea energiei interne și munca efectuată de gaz în acest proces sunt: respectiv:
a) 0 și 50 cal.
b) 50 cal și 0.
c) 0 și 0.
d) 50 cal și -50 cal.
e) 0 și -50 cal.
Modificarea energiei interne este direct legată de schimbarea temperaturii. Deoarece procesul este izoterm, nu există nicio schimbare de temperatură, deci .
Din prima lege a termodinamicii:
Deoarece căldura este eliberată, semnul său este negativ.
intrebarea 9
(UFRN 2012) Biomasa este una dintre principalele surse de energie regenerabilă și, prin urmare, mașinile care o folosesc drept combustibil pentru generarea de energie sunt importante din punct de vedere al mediului. Un exemplu foarte comun este utilizarea biomasei pentru a conduce o turbină cu abur pentru a genera muncă. Figura din lateral prezintă schematic o centrală termoelectrică simplificată.
În această centrală termoelectrică, arderea biomasei în cuptor produce căldură, care încălzește apa din cazan și generează abur de înaltă presiune. Aburul, la rândul său, este condus prin conducte către turbina care, sub acțiunea sa, începe să își rotească palele.
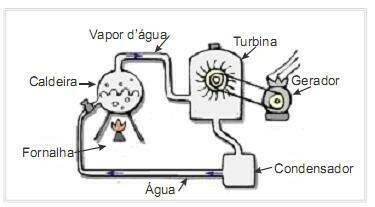
Să presupunem că pierderile de căldură din cauza diferențelor de temperatură dintre piesele acestui motor termic și mediu sunt neglijabile. În acest context, variația energiei interne a apei din cazan
a) este mai mare decât suma căldurii care i se furnizează prin arderea biomasei și a lucrărilor efectuate la turbină.
b) este egală cu suma căldurii ce i se furnizează prin arderea biomasei cu munca efectuată la turbină.
c) este egală cu diferența dintre căldura furnizată acestuia prin arderea biomasei și munca efectuată la turbină.
d) este mai mare decât diferența dintre căldura furnizată acestuia prin arderea biomasei și munca efectuată la turbină.
Apa din cazan primește energie sub formă de căldură din arderea combustibilului și eliberează energie sub formă de lucru efectuat la turbină.
intrebarea 10
(UECE 2021) În ceea ce privește proprietățile gazelor, acordați atenție următoarelor afirmații:
i. Pentru un gaz ideal, energia internă este doar o funcție de presiune.
II. Căldura absorbită de un gaz atunci când își schimbă starea este independentă de proces.
III. Energia internă a unui gaz ideal este doar o funcție de temperatură și este independentă de proces.
IV. Într-o expansiune izotermă a unui gaz ideal, munca efectuată de acesta este egală cu căldura absorbită.
Este corect ceea ce este afirmat doar în
a) I și II.
b) III și IV.
c) I și IV.
d) II și III.
III. CORECT. Energia internă a unui gaz ideal este doar o funcție de temperatură și este independentă de proces.
Modificarea energiei interne este direct legată de schimbarea temperaturii.
Unde n este numărul de moli și R este constanta gazului ideal, fiind constante, doar temperatura determină energia internă a gazului.
IV. CORECT. Într-o expansiune izotermă a unui gaz ideal, munca efectuată de acesta este egală cu căldura absorbită.
Deoarece este izotermă, nu există nicio modificare a temperaturii, deci modificarea energiei interne este zero. După prima lege a termodinamicii:
Aflați mai multe cu:
- Prima lege a termodinamicii
- Termodinamică: legi, concepte, formule și exerciții
- Exerciții de termodinamică
- legea gazelor
ASTH, Rafael. Exerciții ale primei legi a termodinamicii.Tot Materia, [n.d.]. Disponibil in: https://www.todamateria.com.br/exercicios-da-primeira-lei-da-termodinamica/. Acces la:
Vezi și tu
- Exerciții de termodinamică
- Termodinamica
- transformarea adiabatică
- Exerciții de termochimie
- Prima lege a termodinamicii
- Științe ale naturii și tehnologiile lor: Enem
- Energie termală
- A doua lege a termodinamicii


