Polaritatea moleculelor este un aspect foarte important, deoarece caracteristicile substanțelor sunt determinate, printre alți factori, de faptul că moleculele lor sunt polare sau nepolare.
Determinarea polarității unei molecule poate fi efectuată prin intermediul Moment Dipol sau Momentul dipol rezultat, al cărui simbol este 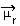 . Dacă vorbim doar despre momentul dipol al fiecărei legături din moleculă, atunci simbolul este litera greacă mi (µ).
. Dacă vorbim doar despre momentul dipol al fiecărei legături din moleculă, atunci simbolul este litera greacă mi (µ).

Molecula va fi nepolare dacă momentul dipolar este egal cu zero, dar dacă este diferit de zero, înseamnă că este polar.

Există două lucruri importante de luat în considerare la determinarea acestui moment dipolar rezultat. Să vedem care sunt:
1) diferență de electronegativitate între atomii elementelor care participă la reacție. De exemplu, molecula HF are o diferență semnificativă în electronegativitate, deoarece fluorul atrage, mult mai mult decât hidrogenul, perechea de electroni din legătură. Astfel, distribuția sarcinilor nu este simetrică, cu dipoli electrici.
Acest dipol este reprezentat de un vector care se confruntă cu capătul care concentrează cei mai mulți electroni, adică de la cel mai mic la cel mai electronegativ atom. Deci, în acest caz, vectorul, care este singurul, va fi vectorul rezultat, așa cum se indică mai jos:
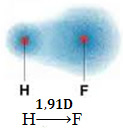
Rețineți că valoarea vectorului este aceeași cu momentul dipolar, care este dat în unitatea debye (D = 3.33. 10-30 coulomb. metrou). Deoarece momentul dipolar este diferit de zero, molecula și legătura sunt polar.
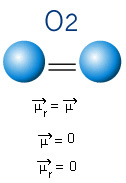
În molecula de mai jos, avem și o moleculă cu doar doi atomi, cu toate acestea, în acest caz, corespunde unei substanțe simple, adică este formată dintr-un singur tip de element. Prin urmare, nu există nicio diferență de electronegativitate; atomii atrag, de asemenea, electroni, care sunt distribuiți simetric. Momentul dipolar rezultat este egal cu zero, deci atât legătura cât și molecula sunt apolar.
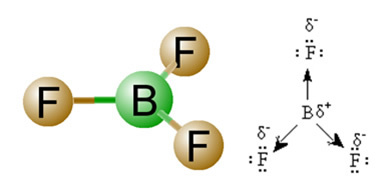
2) Geometria moleculelor, adică dispunerea spațială a vectorilor. Molecula BF3 are trei legături polare, în care fluorul este cel mai electronegativ, având astfel vectorii direcționați spre el. Cu toate acestea, deoarece dispunerea spațială a atomilor este trigonală plană, acest lucru face ca electronii să aibă o distribuție simetrică în jurul atomului central. Astfel, rezultatul este că acești trei vectori se anulează reciproc și momentul dipol este egal cu zero. Prin urmare, molecula BF3 é apolat.
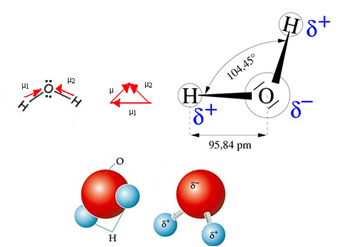
Molecula de apă are doi vectori, cu toate acestea, geometria sa spațială nu este plană, ci sub forma unui V. Rețineți în figura următoare că astfel vectorii lor nu se anulează reciproc, electronii sunt distribuiți asimetric și mai concentrați în cel mai electronegativ atom, care este oxigenul. Astfel, momentul dipol este diferit de zero, iar molecula de apă este polar:
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/momento-dipolar-resultante.htm
