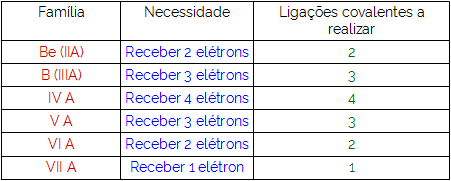
pierwiastek chemiczny fosfor (P) należy do trzeciego okresu układu okresowego i do rodziny azotu (VA). Z tego powodu jego atomy zwykle tworzą trzy wiązania chemiczne dotrzeć do teoria oktetów (stabilność). Istnieją jednak sytuacje, w których atom fosforu tworzy więcej niż trzy wiązania, co jest możliwe tylko dzięki zjawisko hybrydyzacji.
Aby zrozumieć hybrydyzacja fosforu, musimy najpierw zrozumieć, dlaczego atom tego pierwiastka tworzy trzy wiązania. Aby to zrobić, wystarczy monitorować Twoją dystrybucję elektroniczną:

Elektroniczna dystrybucja fosforu
Możemy zaobserwować, że w warstwie walencyjnej atom fosforu ma pełny podpoziom 3s (z dwa elektrony) i niekompletny podpoziom 3p (każdy z trzech orbitali podpoziomu p ma a elektron). Poniżej mamy rozkład elektronów na orbitalach podpoziomów Warstwa walencyjna fosforu:
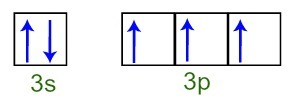
Reprezentacja elektronów powłoki walencyjnej atomu fosforu
Ponieważ każdy z orbitali podpoziomowych 3p jest niekompletny, atom fosforu jest w stanie utworzyć trzy wiązania chemiczne, osiągając w ten sposób stabilność.
Teraz, gdy spojrzymy na substancję PCl5na przykład jesteśmy pewni, że w tej cząsteczce fosfor uległ hybrydyzacji, ponieważ dokonał pięciu połączeń. Ponieważ chlor, który należy do rodziny VIIA, potrzebuje wiązania, aby był stabilny, a cząsteczka ma pięć atomów tego pierwiastek, każdy z nich musi tworzyć wiązanie, co sprawia, że atom fosforu z kolei też musi tworzyć pięć Znajomości. To zdarzenie jest możliwe tylko poprzez only hybrydyzacja (unia niekompletnych orbitali atomowych) fosforu.
Teraz nie przestawaj... Po reklamie jest więcej ;)
Pobierając energię ze środowiska zewnętrznego, elektrony atomu fosforu ulegają wzbudzeniu. Niedługo potem jeden z dwóch elektronów należących do podpoziomu 3s przesuwa się na pusty orbital obecny na podpoziomie d, który do tej pory nie ma żadnych elektronów. Zobacz poniższy schemat:
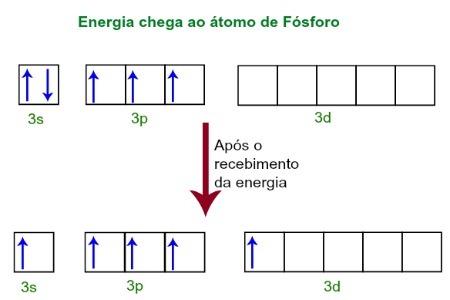
Po otrzymaniu energii elektrony luminoforu są wzbudzone i jeden zajmuje orbitę podpoziomu d.
W tej chwili mamy w warstwie walencyjnej fosforu orbital s, trzy orbitale p i niekompletny orbital d.Ostatecznie te pięć orbitali hybrydyzuje, to znaczy łączą się, w wyniku czego powstaje pięć niekompletnych orbitali atomowych, które są teraz zdolne do tworzenia pięciu wiązań chemicznych.

Hybrydyzacja niekompletnych orbitali atomowych fosforu
Jako orbital s połączono trzy orbitale p i orbital d, hybrydyzacja fosforu jest typu sp3re.
Przeze mnie Diogo Lopes Dias
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
DNI, Diogo Lopes. „Hybrydyzacja fosforu”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm. Dostęp 28 czerwca 2021 r.