Ciepłoutajony jest kwota energiatermiczny który jest wchłaniany lub oddawany przez ciało lub układ termodynamiczny podczas zmiany jego stanu fizycznego, w stała temperatura.
Kiedy czysta substancja osiąga temperaturę Połączenie lub wrzenie, podczas rozgrzewki, twój stan fizyczny zaczyna się zmieniać. W tym procesie nadal pochłania ciepło, jednak jego temperaturapozostajestały. Dzieje się tak, ponieważ po osiągnięciu tych temperatur, w których zachodzą zmiany stanu fizycznego, całe ciepło, które jest pochłaniane przez układ termodynamiczny, jest wykorzystywane do pokonania energiapotencjał który utrzymuje razem jego cząsteczki. Gdy tylko układ termodynamiczny pochłonie całą energię niezbędną do rozbicia jego cząsteczek, interakcja między nimi maleje, co wskazuje, że zmienił się ich stan skupienia. Po zmianie stanu fizycznego ciepło, które zostało wchłonięte izotermicznie nadal jest wchłaniany przez cząsteczki, zapewniając je energiakinetyka. Ten rodzaj ciepła, który zwiększa energię kinetyczną cząsteczek, nazywa się ciepło jawne.
Popatrzrównież: Siedem „złotych” wskazówek, jak efektywniej studiować fizykę
O ciepłoutajony mierzy ilość ciepła, na jednostkę masy, potrzebną do jakiejkolwiek zmiany w stan fizyczny ciała, a więc jego jednostka miary, zgodnie z systemem międzynarodowym (SI), jest Dżulzakilogram (J/kg). Jednak korzystanie z innych jednostek, takich jak kaloriazagram (cal/g), jest dość powszechny w badaniach kalorymetrii.
Rodzaje ciepła utajonego
Istnieją dwa rodzaje ciepła: o ciepłogdybypoziom to jest ciepłoutajony. Ciepło jawne to ciepło, które jest przenoszone między ciałami, gdy występują zmiany temperatury. Z kolei ciepło utajone powstaje, gdy dochodzi do wymiany ciepła bez zmian temperatury.
Ciepło utajone jest zmieniane dla różnych zmian stanu fizycznego. Sprawdź różne rodzaje ciepła utajonego:
Ciepłowpołączenie (Lfa): jest to ciepło, które jest pochłaniane lub oddawane przez ciała podczas procesu stapiania: od cieczy do ciała stałego i odwrotnie, przy stałej temperaturze.
Ciepłowwaporyzacja (LV): to taki, który jest przenoszony podczas przemian ciało stałe-ciecz lub ciecz-ciało stałe, w stała temperatura.
Popatrzrównież: Jaka jest pojemność cieplna?
Przykładywciepłoutajony
Sprawdź kilka codziennych sytuacji, w których dochodzi do utajonej wymiany ciepła:
Gdy podgrzewamy wodę do temperatury 100°C, rozpoczyna się proces parowania. Dopóki woda nie zamieni się w parę, jej temperatura się nie zmieni.
Gdy wlewamy wodę na bardzo gorącą powierzchnię, cała woda niemal natychmiast wyparowuje. Proces ten nazywa się ogrzewaniem i obejmuje pochłanianie ciepła utajonego.
Gdy dotykamy butelki po napojach gazowanych w niskich temperaturach i całej jej zawartości, następuje utajona wymiana ciepła zamarza szybko w stałej temperaturze, dzięki temperaturze niższej niż temperatura topnienia wody.
formuła ciepła utajonego
Ciepło utajone oblicza się jako stosunek ilości ciepła przekazanego w przemianie izotermicznej:
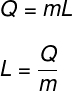
Q – ilość przekazanego ciepła
m – masa ciała
L - Ciepło
Zmiany fazowe i ciepło utajone
W czystych substancjach następują zmiany fazowe wtemperaturastały, poprzez absorpcję lub uwalnianie ciepła utajonego. Wszystkie czyste substancje mają krzywa grzewcza podobny do zdjęcia poniżej:
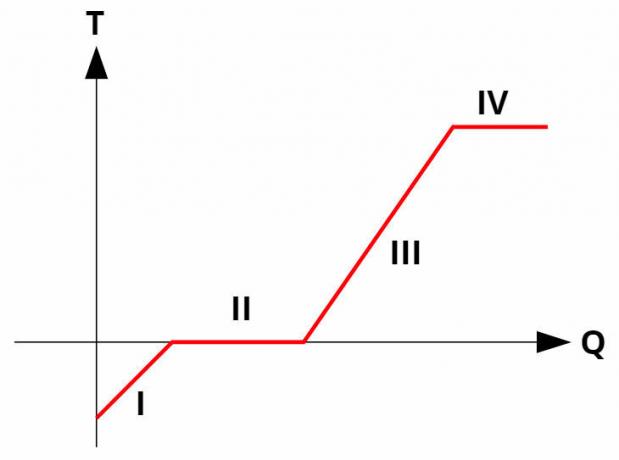
W Krzywewogrzewanie powiązać temperaturę (oś y) z ilością ciepła oddanego lub odebranego (oś x). W przemianach fazowych (procesy II i IV) temperatura pozostaje stała, chociaż nadal zachodzi wymiana ciepła.
Zobacz też: Podstawy kalorymetrii
stół ciepła utajonego
W normalnych warunkach temperatura i nacisk, O ciepłoutajony wody, ze względu na różne zmiany jej stanu fizycznego, przedstawia poniższa tabela:
Transformacja |
Ciepło utajone (cal/g) |
Fuzja (0°C) |
80 |
Krzepnięcie (0°C) |
-80 |
Parowanie (100°C) |
540 |
Kondensacja (100°C) |
-540 |
Zgodnie z powyższą tabelą, 80kalorie zamrażać 1 gramwody o temperaturze topnienia (0 °C). Negatywne znaki w procesy zestalenie i kondensacja wskazują, że zostało w nich uwolnione ciepło, więc te dwie przemiany są egzotermiczny. Poniższa tabela przedstawia ciepło utajone w J/kg, dla tych samych procesów:
Transformacja |
Ciepło utajone (J/kg) |
Fuzja (0°C) |
333.103 |
Krzepnięcie (0°C) |
-333.103 |
Parowanie (100°C) |
2,2.106 |
Kondensacja (100°C) |
-2,2.106 |

ćwiczenia z ciepła utajonego
1) Jeden pojemnik mieści 500 g płynnej wody. Bez zmian temperatury wody cała jej zawartość zostaje nagle odparowana. Określ, ile ciepła przeszło do zawartości tego pojemnika.
Dane: Lfa = 540 kcal/g
Rozkład:
Aby obliczyć ilość ciepła potrzebną do odparowania tej masy wody, użyjemy następującego wzoru:
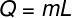
Korzystając z danych dostarczonych w ćwiczeniu, dokonamy następujących obliczeń:
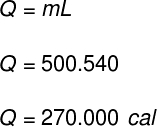
Przeze mnie Rafael Helerbrock



