Różne substancje istniejące we wszechświecie składają się z atomów, jonów lub cząsteczek. Pierwiastki chemiczne łączą się poprzez wiązania chemiczne. Te linki mogą być:
| Wiązanie kowalencyjne | wiązanie jonowe | Połączenie metalowe |
|---|---|---|
współdzielenie elektronów |
przeniesienie elektronu |
Między atomami metali |
Skorzystaj z poniższych pytań, aby sprawdzić swoją wiedzę na temat wiązań chemicznych.
Proponowane ćwiczenia
Pytanie 1
Aby zinterpretować właściwości różnych substancji, konieczne jest poznanie wiązań między atomami i wiązań między odpowiednimi cząsteczkami. W odniesieniu do wiązania między atomami można powiedzieć, że…
(A) pomiędzy związanymi atomami przeważają siły przyciągania.
(B) gdy tworzy się wiązanie między atomami, utworzony układ osiąga maksymalną energię.
(C) przyciąganie i odpychanie w cząsteczce ma nie tylko charakter elektrostatyczny.
(D) pomiędzy związanymi atomami istnieje równowaga między przyciąganiem elektrostatycznym a odpychaniem.
Prawidłowa alternatywa: (D) Pomiędzy związanymi atomami istnieje równowaga między przyciąganiem elektrostatycznym a odpychaniem.
Atomy powstają z ładunków elektrycznych i to siły elektryczne między cząstkami prowadzą do powstania wiązań. Dlatego wszystkie wiązania chemiczne mają charakter elektrostatyczny.
Atomy mają siły:
- odpychanie między jądrami (ładunki dodatnie);
- odpychanie między elektronami (ładunki ujemne);
- przyciąganie między jądrami a elektronami (ładunki dodatnie i ujemne).
We wszystkich układach chemicznych atomy dążą do stania się bardziej stabilnymi, a stabilność tę osiąga się w wiązaniu chemicznym.
Stabilność wynika z równowagi między siłami przyciągania i odpychania, ponieważ atomy osiągają stan niższej energii.
pytanie 2
Prawidłowo dopasuj zdania w kolumnie I i typ powiązania w kolumnie II.
| ja | II |
|---|---|
| (A) Między atomami Na | 1. pojedyncze wiązanie kowalencyjne |
| (B) Między atomami Cl | 2. podwójne wiązanie kowalencyjne |
| (C) Między atomami O | 3. Połączenie metalowe |
| (D) Między N atomami | 4. wiązanie jonowe |
| (E) Między atomami Na i ClCl | 5. potrójne wiązanie kowalencyjne |
Odpowiadać:
Atomy |
Typy połączeń |
Reprezentacja |
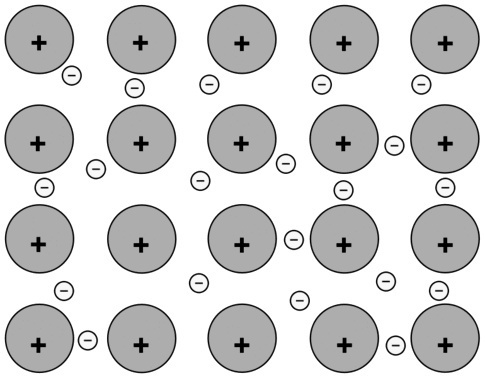
(A) Między atomami Na |
Metaliczne połączenie. Atomy tego metalu są połączone wiązaniami metalicznymi, a oddziaływanie między ładunkami dodatnimi i ujemnymi zwiększa stabilność zestawu. |
 |
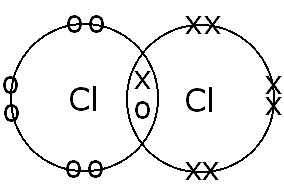
(B) Między atomami Cl |
Pojedyncze wiązanie kowalencyjne. Dzielenie się elektronami i tworzenie pojedynczego wiązania występuje, ponieważ istnieje tylko jedna para elektronów wiążących. |
 |
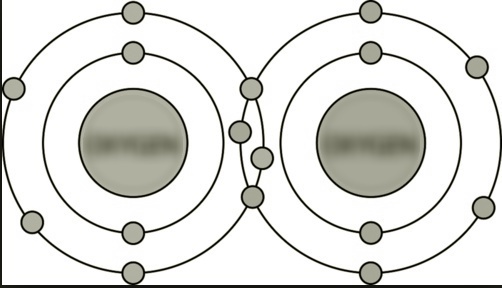
(C) Między atomami O |
Podwójne wiązanie kowalencyjne. Istnieją dwie pary elektronów wiążących. |
 |
(D) Między N atomami |
Potrójne wiązanie kowalencyjne. Istnieją trzy pary elektronów wiążących. |
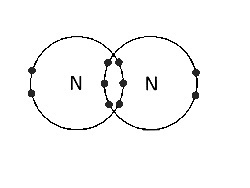 |
(E) Między atomami Na i ClCl |
Wiązanie jonowe. Ustanowiony między jonami dodatnimi (kationami) i jonami ujemnymi (aniony) poprzez przeniesienie elektronów. |
 |
pytanie 3
Metan, amoniak, woda i fluorowodór to substancje molekularne, których struktury Lewisa przedstawiono w poniższej tabeli.
| Metan, CH4 | amoniak, NH,3 | Woda, H2O | fluorowodór, HF |
|---|---|---|---|
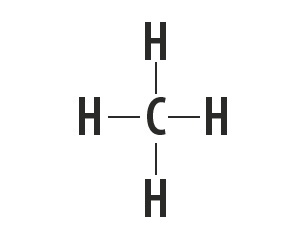 |
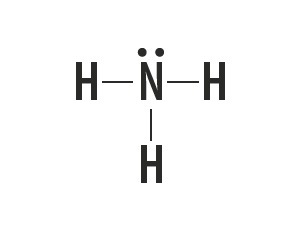 |
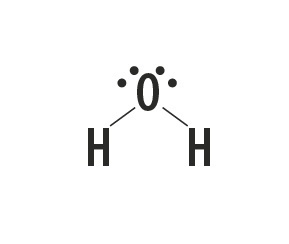 |
 |
Wskazuje rodzaj wiązania ustanowionego między atomami tworzącymi te cząsteczki.
Prawidłowa odpowiedź: Proste wiązanie kowalencyjne.
Patrząc na układ okresowy widzimy, że pierwiastki substancji nie są metalami.
Rodzaj wiązania, jakie te pierwiastki tworzą między nimi, to wiązanie kowalencyjne, ponieważ dzielą one elektrony.
Atomy węgla, azotu, tlenu i fluoru tworzą osiem elektronów w powłoce walencyjnej ze względu na liczbę wiązań, jakie tworzą. Następnie przestrzegają zasady oktetu.
Z drugiej strony wodór uczestniczy w tworzeniu substancji molekularnych, dzieląc parę elektronów, tworząc proste wiązania kowalencyjne.
Zobacz też: Wiązania chemiczne
pytania egzaminacyjne
Pytania dotyczące wiązań chemicznych pojawiają się często na egzaminach wstępnych na studia. Zobacz poniżej, jak można podejść do tematu.
Pytanie 1
(UEMG) Właściwości wykazywane przez określony materiał można wytłumaczyć rodzajem wiązania chemicznego występującego między jego jednostkami tworzącymi. W analizie laboratoryjnej chemik zidentyfikował następujące właściwości określonego materiału:
- Wysoka temperatura topnienia i wrzenia
- Dobra przewodność elektryczna w roztworze wodnym
- Zły przewodnik elektryczności półprzewodnikowej
Z właściwości wyświetlanych przez ten materiał zaznacz alternatywę, która wskazuje dominujący w nim typ połączenia:
(A) metaliczny
(B) kowalencyjne
(C) indukowany dipol
(D) jonowy
Prawidłowa alternatywa: (D) jonowy.
Materiał stały ma wysoką temperaturę topnienia i wrzenia, co oznacza, że do przejścia w stan ciekły lub gazowy potrzebowałby dużo energii.
W stanie stałym materiał jest słabym przewodnikiem elektryczności ze względu na organizację atomów, które tworzą dobrze określoną geometrię.
W kontakcie z wodą pojawiają się jony, tworząc kationy i aniony, ułatwiające przepływ prądu elektrycznego.
Rodzaj wiązania, który sprawia, że materiał posiada te właściwości, to wiązanie jonowe.
pytanie 2
(PUC-SP) Przeanalizuj właściwości fizyczne w poniższej tabeli:
| Próba | Punkt fuzji | Temperatura wrzenia | Przewodność elektryczna w 25°C | Przewodność elektryczna w 1000 °C |
|---|---|---|---|---|
| TEN | 801°C | 1413°C | izolacyjny | konduktor |
| b | 43°C | 182 °C | izolacyjny | |
| DO | 1535 °C | 2760°C | konduktor | konduktor |
| re | 1248°C | 2250 °C | izolacyjny | izolacyjny |
Zgodnie z modelami wiązań chemicznych, A, B, C i D można sklasyfikować odpowiednio jako:
(A) związek jonowy, metal, substancja molekularna, metal.
(B) metal, związek jonowy, związek jonowy, substancja molekularna.
(C) związek jonowy, substancja molekularna, metal, metal.
(D) substancja molekularna, związek jonowy, związek jonowy, metal.
(E) związek jonowy, substancja molekularna, metal, związek jonowy.
Właściwa alternatywa: (E) związek jonowy, substancja molekularna, metal, związek jonowy.
Analizując stany fizyczne próbek pod wpływem przedstawionych temperatur, musimy:
| Próba | Stan fizyczny w 25°C | Stan fizyczny w 1000°C | Klasyfikacja związków |
| TEN | solidny | ciekły | joński |
| b | solidny | Molekularny | |
| DO | solidny | solidny | Metal |
| re | solidny | solidny | joński |
Oba związki A i D są izolatorami w stanie stałym (w temperaturze 25°C), ale gdy próbka A przechodzi w stan ciekły, staje się przewodząca. Są to cechy charakterystyczne związków jonowych.
Związki jonowe w stanie stałym nie pozwalają na przewodnictwo ze względu na sposób, w jaki atomy się układają.
W roztworze związki jonowe zamieniają się w jony i umożliwiają przewodzenie elektryczności.
Metale charakteryzują się dobrą przewodnością, jak próbka C.
Związki molekularne są elektrycznie obojętne, to znaczy izolatory jak próbka B.
Zobacz też: Metalowe linki
pytanie 3
(Fuvest) Rozważmy pierwiastki tworzące chlor, odpowiednio z wodorem, węglem, sodem i wapniem. Z którym z tych pierwiastków chlor tworzy związki kowalencyjne?
Odpowiadać:
| Elementy | Jak odbywa się połączenie | utworzona więź | |
| chlor | Wodór | 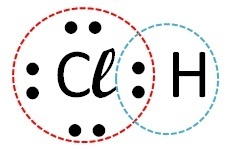 |
Kowalencyjne (współdzielenie elektronów) |
| chlor | Węgiel | 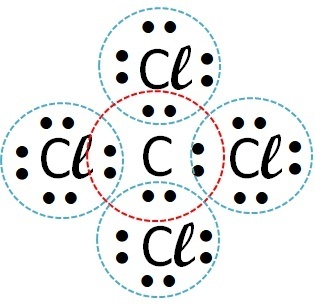 |
Kowalencyjne (współdzielenie elektronów) |
| chlor | Sód |  |
Jonowe (przenoszenie elektronów) |
| chlor | Wapń | 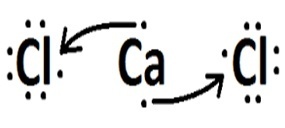 |
Jonowe (przenoszenie elektronów) |
Związki kowalencyjne występują w interakcji atomów niemetali, niemetali z wodorem lub między dwoma atomami wodoru.
Tak więc wiązanie kowalencyjne występuje z chlorem + wodorem i chlorem + węgiel.
Sód i wapń są metalami i wiążą się z chlorem poprzez wiązanie jonowe.
Pytania dotyczące Enem
Podejście Enema do tematu może się nieco różnić od tego, co widzieliśmy do tej pory. Zobacz, jak pojawiły się wiązania chemiczne w teście 2018 i dowiedz się nieco więcej o tej treści.
Pytanie 1
(Enem/2018) Badania pokazują, że nanourządzenia oparte na ruchach atomowych, indukowanych przez lekkie, mogą mieć zastosowanie w przyszłych technologiach, zastępując mikrosilniki, bez konieczności stosowania komponentów mechanika. Przykład ruchu molekularnego wywołanego światłem można zobaczyć, wyginając cienki wafel krzemowy, związany z polimerem azobenzenowym i materiałem nośnika, w dwóch długościach fal, jak pokazano na postać. Przy zastosowaniu światła zachodzą odwracalne reakcje łańcucha polimerowego, które sprzyjają obserwowanemu ruchowi.
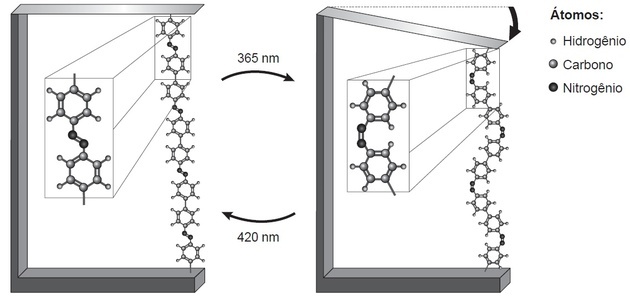
WEŹ, H. I. Nanotechnologia cząsteczek. Nowa Chemia w Szkole, nr. 21 maja 2005 (dostosowany).
Zjawisko ruchu molekularnego, promowane przez padanie światła, wynika z (a)
(A) ruch wibracyjny atomów, który prowadzi do skrócenia i rozluźnienia wiązań.
(B) izomeryzacja wiązań N=N, przy czym forma cis polimeru jest bardziej zwarta niż forma trans.
(C) tautomeryzacja jednostek monomerycznych polimeru, która prowadzi do bardziej zwartego związku.
(D) rezonans pomiędzy elektronami π grupy azowej a elektronami pierścienia aromatycznego skracającymi wiązania podwójne.
(E) zmienność konformacyjna wiązań N=N, w wyniku której powstają struktury o różnych polach powierzchni.
Prawidłowa alternatywa: (B) izomeryzacja wiązań N=N, forma cis polimeru jest bardziej zwarta niż trans.
Ruch w łańcuchu polimeru powoduje, że po lewej stronie obserwuje się dłuższy polimer, a po prawej krótszy.
Z podświetloną częścią polimerową obserwujemy dwie rzeczy:
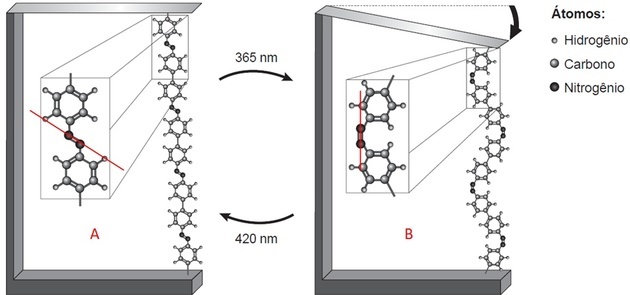
- Istnieją dwie struktury, które są połączone wiązaniem między dwoma atomami (które legenda wskazuje, że to azot);
- Ten link znajduje się w różnych pozycjach na każdym obrazie.
Rysując linię na obrazie, w A obserwujemy, że struktury znajdują się powyżej i poniżej osi, czyli po przeciwnych stronach. W B znajdują się po tej samej stronie narysowanej linii.
Azot tworzy trzy wiązania, aby były stabilne. Jeśli jest przyłączony do struktury wiązaniem, wiąże się z innym azotem poprzez kowalencyjne wiązanie podwójne.
Zagęszczanie polimeru i zginanie ostrzy następuje, ponieważ spoiwa znajdują się w różnych pozycjach, gdy występuje izomeria wiązań N=N.
Izomerię trans obserwuje się w A (linkery po przeciwnych stronach) i cis w B (linkery w tej samej płaszczyźnie).
pytanie 2
(Enem/2018) Niektóre materiały stałe składają się z atomów, które oddziałują ze sobą, tworząc wiązania kowalencyjne, jonowe lub metaliczne. Rysunek przedstawia potencjalną energię wiązania w funkcji odległości międzyatomowej w krystalicznym ciele stałym. Analizując ten rysunek, można zaobserwować, że w temperaturze zero kelwinów równowagowa odległość wiązania między atomami (R0) odpowiada minimalnej wartości energii potencjalnej. Powyżej tej temperatury energia cieplna dostarczana do atomów zwiększa ich energię kinetyczną i powoduje oscylują wokół średniej pozycji równowagi (wypełnione kółka), która dla każdego jest inna temperatura. Odległość połączenia może zmieniać się na całej długości linii poziomych, identyfikowanych wartością temperatury T1 T4 (rosnące temperatury).
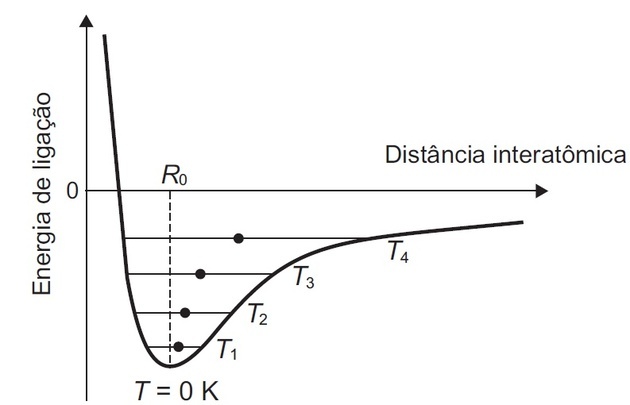
Przemieszczenie obserwowane w średniej odległości ujawnia zjawisko
(A) jonizacja.
(B) rozszerzenie.
(C) dysocjacja.
(D) zerwanie wiązań kowalencyjnych.
(E) tworzenie wiązań metalicznych.
Prawidłowa alternatywa: (B) rozszerzenie.
Atomy mają ładunki dodatnie i ujemne. Wiązania tworzą się, gdy osiągną minimalną energię, równoważąc siły (odpychanie i przyciąganie) między atomami.
Z tego rozumiemy, że: aby wystąpiło wiązanie chemiczne, istnieje idealna odległość między atomami, aby były stabilne.
Przedstawiona grafika pokazuje nam, że:
- Odległość między dwoma atomami (międzyatomowymi) zmniejsza się aż do osiągnięcia minimalnej energii.
- Energia może wzrosnąć, gdy atomy zbliżą się tak blisko, że ładunki dodatnie w ich jądrach zbliżą się do siebie, zaczynają się od siebie odpychać, a w konsekwencji zwiększają energię.
- W temperaturze T0 zero Kelvin jest minimalną wartością energii potencjalnej.
- Następuje wzrost temperatury T1 do T4 a dostarczana energia powoduje, że atomy oscylują wokół pozycji równowagi (wypełnione kółka).
- Oscylacja występuje między krzywą a pełnym okręgiem odpowiadającym każdej temperaturze.
Ponieważ temperatura mierzy stopień poruszenia cząsteczek, im wyższa temperatura, tym bardziej atom oscyluje i zwiększa się zajmowana przez niego przestrzeń.
Najwyższa temperatura (T4) wskazuje, że ta grupa atomów będzie zajmowała większą przestrzeń, a tym samym materiał się rozszerza.
pytanie 3
(Enem/2019) Ponieważ mają kompletną warstwę walencyjną, wysoką energię jonizacji i powinowactwo elektroniczne praktycznie zerowa, przez długi czas uważano, że gazy szlachetne nie tworzą związków środki chemiczne. Jednak w 1962 r. udało się przeprowadzić reakcję ksenonu (warstwa walencyjna 5s²5p⁶) z sześciofluorkiem platyny i od tego czasu zsyntetyzowano więcej nowych związków gazów szlachetnych.
Takie związki pokazują, że nie można bezkrytycznie przyjąć reguły oktetu, w której uważa się, że w wiązaniu chemicznym atomy mają tendencję do uzyskiwania stabilności przy założeniu konfiguracji elektronowej gazu szlachetny. Wśród znanych związków jednym z najbardziej stabilnych jest difluorek ksenonu, w którym dwa atomy halogenu fluor (warstwa walencyjna 2s²2p⁵) wiąże się kowalencyjnie z atomem gazu szlachetnego, aby mieć osiem elektronów wartościowość.
Ile elektronów znajduje się w powłoce walencyjnej atomu gazu szlachetnego, pisząc wzór Lewisa dla wspomnianego związku ksenonowego?
(A) 6
(B) 8
(C) 10
(D) 12
Prawidłowa alternatywa: c) 10.
Fluor jest pierwiastkiem należącym do grupy 17 układu okresowego. Dlatego w jego najbardziej zewnętrznej powłoce elektronicznej znajduje się 7 elektronów (2s2 2p5). Aby uzyskać stabilność, zgodnie z zasadą oktetu, atom tego pierwiastka potrzebuje jednego elektronu, aby mieć 8 elektronów w powłoce walencyjnej i przyjąć konfigurację elektronową gazu szlachetnego.
Z kolei ksenon jest gazem szlachetnym, a zatem ma już 8 elektronów w ostatniej warstwie (5s2 5p6).
Zauważ, że nazwa związku to difluorek ksenonu, co oznacza, że związek składa się z dwóch atomów fluoru i jednego atomu ksenonu, XeF2.
Jak mówi stwierdzenie, wiązanie chemiczne między atomami jest typu kowalencyjnego, to znaczy istnieje współdzielenie elektronów.
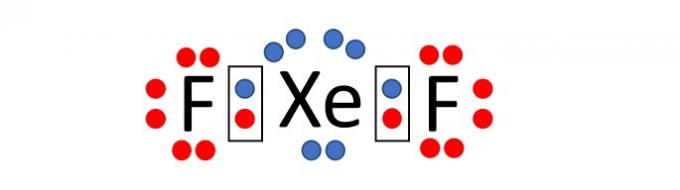
Rozprowadzając elektrony wokół każdego atomu (7 wokół fluoru i 8 wokół ksenonu) widzimy że atom ksenonu, gdy łączy się z dwoma atomami fluoru, ma 10 elektronów w powłoce fluorowej. wartościowość.
Zobacz też:
- reguła oktetu
- Ćwiczenia z dystrybucji elektronicznej
- Ćwiczenia na węglowodorach