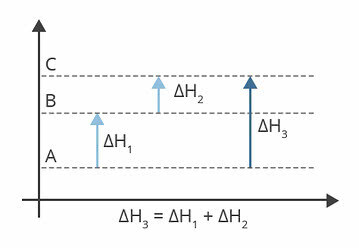
Entalpia to ilość energii w danej reakcji, możemy obliczyć ciepło układu poprzez zmianę entalpii (∆H).
∆H w stanie fizycznym zmienia się: 
Rysunek przedstawia zmianę stanu fizycznego ze stałego na ciekły (topienie). Występuje, gdy woda ulega entalpii topnienia: topnienia lodu w wyniku absorpcji ciepła. Ilość ciepła potrzebna do zajścia tego procesu wynosi 7,3 KJ/mol (stopienie 1 mola H2Ty)). Równanie procesu:
H2O(y) → H2(1) ∆H = + 7,3 KJ/mol
Teraz nie przestawaj... Po reklamie jest więcej ;)
Teraz zwróć uwagę na poniższy obrazek:
Zwróć uwagę, że para wydobywająca się z czajnika pokazuje zmianę stanu fizycznego. Woda wewnątrz czajnika była w stanie ciekłym, ale w wyniku absorpcji ciepła przeszła w stan gazowy. Ciepło wymagane do zajścia entalpii parowania w 1 mol H2O(1) wynosi 44 KJ/mol, zgodnie z równaniem:
H2O (1) → H2(v) ∆H = + 44 KJ/mol
Liria Alves
Absolwent chemii
Brazylijska drużyna szkolna
Fizykochemiczne - Chemia - Brazylia Szkoła
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
SOUZA, Líria Alves de. „Entalpia zmian stanu fizycznego”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/entalpia-nas-mudancas-estado-fisico.htm. Dostęp 28 czerwca 2021 r.