Prawo Hessa pozwala nam obliczyć zmienność entalpii, czyli ilość energii obecnej w substancjach po przejściu reakcji chemicznych. Dzieje się tak, ponieważ nie można zmierzyć samej entalpii, ale jej zmienności.
Prawo Hessa leży u podstaw badań nad termochemią.
Prawo to zostało eksperymentalnie opracowane przez Germaina Henry'ego Hessa, który ustanowił:
Zmiana entalpii (ΔH) w reakcji chemicznej zależy tylko od stanu początkowego i końcowego reakcji, niezależnie od liczby reakcji.
Jak obliczyć prawo Hessa?
Zmianę entalpii można obliczyć odejmując entalpię początkową (przed reakcją) od entalpii końcowej (po reakcji):
ΔH = Hfa - Hja
Innym sposobem obliczenia tego jest suma entalpii w każdej z reakcji pośrednich. Bez względu na liczbę i rodzaj reakcji.
ΔH = ΔH1 + ΔH2
Ponieważ to obliczenie uwzględnia tylko wartości początkowe i końcowe, stwierdza się, że energia pośrednia nie wpływa na wynik jej zmiany.
To jest szczególny przypadek Zasada oszczędzania energii, a Pierwsza zasada termodynamiki.
Powinieneś także wiedzieć, że prawo Hessa można obliczyć jako równanie matematyczne. Aby to zrobić, możesz wykonać następujące czynności:
- Odwróć reakcję chemiczną, w tym przypadku znak ΔH również musi zostać odwrócony;
- Pomnóż równanie, należy również pomnożyć wartość ΔH;
- Podziel równanie, wartość ΔH również musi zostać podzielona.
dowiedz się więcej o entalpia.
Wykres entalpii
Prawo Hessa można również zwizualizować za pomocą diagramów energetycznych:
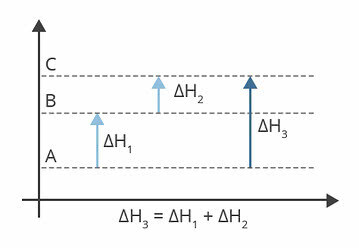
Powyższy diagram pokazuje poziomy entalpii. W tym przypadku doznane reakcje są endotermiczne, to znaczy zachodzi absorpcja energii.
H1 to zmiana entalpii, która zachodzi od A do B. Załóżmy, że to 122 kj.
H2 to zmiana entalpii, która zachodzi od B do C. Załóżmy, że jest to 224 kj.
H3 to zmiana entalpii, która zachodzi od A do C.
Dlatego ważne jest dla nas, aby znać wartość ΔH3, ponieważ odpowiada to zmianie entalpii reakcji od A do C.
Możemy znaleźć wartość ΔH3, z sumy entalpii w każdej z reakcji:
H3 = ΔH1 + ΔH2
H3 = 122 kj + 224 kj
H3 = 346 kj
Lub ΔH = Hfa - Hja
ΔH = 346 kj – 122 kj
ΔH = 224 kj
Egzamin wstępny: rozwiązany krok po kroku
1. (Fuvest-SP) Na podstawie zmian entalpii związanych z następującymi reakcjami:
N2(g) + 2 O2(g) → 2 NIE2(g) ∆H1 = +67,6 kJ
N2(g) + 2 O2(g) → N2O4(g) ∆H2 = +9,6 kJ
Można przewidzieć, że zmienność entalpii związana z reakcją dimeryzacji NO2 będzie równa:
2 NO2(g) → 1 N2O4(g)
a) -58,0 kJ b) +58,0 kJ c) -77,2 kJ d) +77,2 kJ e) +648 kJ
Rozkład:
Krok 1: Odwróć pierwsze równanie. To dlatego, że NIE2(g) musi przejść na stronę reagentów, zgodnie z globalnym równaniem. Pamiętaj, że odwracając reakcję, ∆H1 odwraca również znak, zmieniając go na ujemny.
Drugie równanie jest zachowane.
2 NIE2(g) → N2(g) + 2 O2(g) ∆H1 = - 67,6 kJ
N2(g) + 2 O2(g) → N2O4(g) ∆H2 = +9,6 kJ
Krok 2: Zauważ, że N2(g) pojawia się w produktach i odczynnikach i to samo dzieje się z 2 molami O2(g).
2 NIE2(g) → N2(g)+ 2 O2(g)∆H1 = - 67,6 kJ
N2(g) + 2 O2(g) → N2O4(g) ∆H2 = +9,6 kJ
W ten sposób można je anulować, co daje następujące równanie:
2 NIE2(g) → N2O4(g).
Krok 3: Widać, że doszliśmy do globalnego równania. Teraz musimy dodać równania.
∆H = ∆H1 + ∆H2
∆H = - 67,6 kJ + 9,6 kJ
∆H = -58 kJ ⇒ Alternatywa A
Z ujemnej wartości ∆H wiemy również, że jest to reakcja egzotermiczna, z wydzieleniem ciepła.
Dowiedz się więcej, czytaj też:
- Termochemia
- Ćwiczenia z termochemii
- Reakcje endotermiczne i egzotermiczne
- Druga zasada termodynamiki
Ćwiczenia
1. (UDESC-2012) Metan może być używany jako paliwo, jak pokazano w równaniu 1:
CH4(g) + 2O2(g) → CO2(g) + 2 godz2O(sol)
Korzystając z poniższych równań termochemicznych, które uznasz za konieczne, oraz pojęć prawa Hessa, uzyskaj wartość entalpii równania 1.
DO(y) + H2O(sol) → CO(sol) + H2(g) ΔH = 131,3 kJ mol-1
WSPÓŁ(sol) + ½2(g) → CO2(g) ΔH = – 283,0 kJ mol-1
H2(g) + ½2(g) → H2O(sol) ΔH = – 241,8 kJ mol-1
DO(y) + 2 godz2(g) → CH4(g) ΔH = – 74,8 kJ mol-1
Wartość entalpii równania 1, w kJ, wynosi:
a) - 704,6
b) - 725,4
c) - 802,3
d) - 524,8
e) - 110,5
c) – 802,3
2. (UNEMAT-2009) Prawo Hessa ma fundamentalne znaczenie w badaniach termochemii i można je stwierdzić ponieważ „zmiana entalpii w reakcji chemicznej zależy tylko od stanu początkowego i końcowego reakcja". Jedną z konsekwencji prawa Hessa jest to, że równania termochemiczne mogą być traktowane algebraicznie.
Biorąc pod uwagę równania:
DO (grafit) + O2(g) → CO2(g) H1 = -393,3 kj
DO (Diament) + O2(g) → CO2(g) H2 = -395,2 kj
W oparciu o powyższe informacje oblicz zmianę entalpii węgla grafitowego na węgiel diamentowy i zaznacz właściwą alternatywę.
a) -788,5 kj
b) +1,9 kj
c) +788,5 kj
d) -1,9 kj
e) +98,1 kj
b) +1,9 kj