Poniżej znajdują się niektóre z podstawowe koncepcje o czym musimy wiedzieć, rozpoczynając studia w Chemia ogólna. Obserwuj je:
→ Chemia
To nauka bada materię, jej przemiany i energie zaangażowane w te procesy. Działa na trzech głównych poziomach:
- Mikroskopowe:
Kiedy chemia interpretuje zjawiska, w których następuje zmiana kolejności atomów, które są podstawowymi składnikami wszelkiej materii i które są niewidoczne dla naszych oczu.
- Makroskopowe:
Kiedy chemia interpretuje duże, widoczne obiekty lub zjawiska.
- Symboliczne:
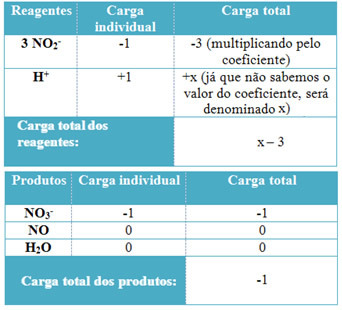
Gdy chemia interpretuje i rozpoznaje zjawiska chemiczne za pomocą symboli, wzorów i równań matematycznych.
* W zależności od kierunku studiów Chemia można podzielić na: Chemia organiczna, Chemia nieorganiczna, Fizykochemiczne, miedzy innymi.
→ Temat
Pomimo tego, że nie jest to tak łatwe do zdefiniowania pojęcie, większość autorów zgadza się, że materia w nauce chemii to wszystko, co zajmuje przestrzeń, przedstawiając objętość i masę.
Przykład: drzewo, powietrze, woda, chmury, nasze własne ciało, ziemia, wszystko to są przykłady materii. Ale na przykład sprawiedliwość nie jest.
→ Makaron
Jest to ogólna właściwość materii, która wskazuje ilość materii, która istnieje w ciele i której standardową jednostką jest kilogram. Do pomiaru tej właściwości stosuje się wagi.
→ Głośność
Jest to również ogólna właściwość materii, która wskazuje wielkość przestrzeni zajmowanej przez ciało, domyślną jednostką jest metr sześcienny (m3). Objętość materiału można mierzyć za pomocą różnych urządzeń z podziałką, takich jak zlewka, pipeta, biureta i inne mniej dokładne.
→Ciało
To ograniczona część sprawy. Na przykład, jak stwierdzono, drzewo jest sprawą; tak więc, kiedy tniemy kłody drewna, mamy, że te kłody mogą być oznaczone jako ciała lub również jako materia.
→Obiekt
Jest to ciało stworzone na użytek człowieka. Jeśli drewniane kłody, o których mowa w poprzednim punkcie, zostaną przerobione na jakieś meble, takie jak stół, będziemy mieli przedmiot.

Przykłady pojęć chemii - materia, ciało i przedmiot
→ Energia
Jest miarą zdolności do wykonywania pracy. Istnieją różne rodzaje energii, w zależności od rodzaju wykonywanej pracy. Na przykład energia, którą ciało nabywa, gdy jest w ruchu, to i isenergia kinetyczna. Energia, którą magazynuje ciało, to energia potencjalna. TEN energia mechaniczna jest to dowolna forma energii związana z ruchem ciał lub zdolnością do wprawiania ich w ruch lub ich deformowania. TEN energia chemiczna opiera się na sile przyciągania i odpychania w wiązaniach chemicznych obecnych w tworzeniu materii. Wymiany ciepła są energie cieplne. Przewodzenie elektryczności to Elektryczność, a energia w postaci światła jest energia świetlna.
Teraz nie przestawaj... Po reklamie jest więcej ;)
→ czysta substancja lub po prostu substancja
Substancje to materiały, które mają wszystkie właściwości fizyczne dobrze zdefiniowane, określone i praktycznie stałe, to znaczy utworzone przez jeden rodzaj składnika (atomy, cząsteczki lub klastry jonowe).
- prosta substancja:
Jest to substancja utworzona przez jeden rodzaj pierwiastek chemiczny. Przykłady: gazowy tlen (O2), gazowy wodór (H2), żelazo (Fe), gaz hel (He), aluminium (Aℓ) itp.
- substancja złożona lub złożony:
Jest to substancja utworzona przez więcej niż jeden pierwiastek chemiczny. Przykłady: woda (H2O), alkohol etylowy lub etanol (C2H5OH), amoniak (NH3) itp.
→ Mieszanki
Kiedy mamy więcej niż jedną substancję w tym samym systemie. Mieszaniny nie mają właściwości, takich jak temperatura topnienia i wrzenia, a także gęstość, które są stałe jak w przypadku substancji.
- Jednorodna mieszanina:
Jest to mieszanina jednofazowa, czyli całkowicie jednorodny wygląd. Przykład: Mieszanina wody i alkoholu.
- Mikstura heterogeniczna:
Jest to mieszanina, która ma więcej niż jedną fazę. Przykład: woda i olej.
→ System
To jest to, co podlega obserwacji. Regiony wokół systemu nazywane są sąsiedztwami.

System jest tym, co jest pod obserwacją
- Jednorodny system:
Zawiera jedną fazę. Może składać się z czystej substancji lub jednorodnej mieszaniny.
- System heterogeniczny:
Zawiera więcej niż jedną fazę. Może składać się z czystej substancji w różnych stanach fizycznych, takiej jak szklanka wody i lodu, lub z mieszaniny niejednorodnej.
→ Zjawisko
Każda przemiana, której dokonała materia.
- zjawiska fizyczne:
Są to takie, w których konstytucja materiału się nie zmienia. Przykład: Zgnij papier.
- zjawiska chemiczne:
To takie, w których zmienia się konstytucja materiału. Przykład: spalanie papieru.
Więcej szczegółów na temat tych pojęć i innych, takich jak atomy, pierwiastki chemiczne i cząsteczki, można znaleźć w innych tekstach na naszej stronie internetowej.
Jennifer Fogaça
Absolwent chemii
Chemia
Substancje molekularne, temperatura wrzenia, powierzchnia kontaktu, temperatura wrzenia, międzycząsteczkowe siły przyciągania, wiązanie chemiczne, związki molekularne, kowalencyjne wiązania chemiczne, wiązania jonowe, wiązania metaliczne, stany fizyczne zły