Halogeneringsreaksjoner er en type organisk substitusjonsreaksjon, det vil si de der en atom eller grupper av atomer erstattes av atomer eller grupper av atomer av et annet molekyl organisk.
Generelt foregår denne typen reaksjon med alkaner og aromatiske hydrokarboner (benzen og dets derivater).
Halogenering er såkalt fordi det forekommer med de enkle stoffene i halogener: F2, Cl2, br2 Hei2. Imidlertid er de vanligste blant disse klorering (Cl2) og bromering (Br2), ettersom fluor er veldig reaktivt, og reaksjonene er eksplosive og vanskelige å kontrollere, og til og med ødelegger organisk materiale:
CH4 (g) + 2 F.2 (g) → C(s) + 4HF(g)
Reaksjoner med jod er ekstremt langsomme.
Nedenfor er hovedtyper av halogenering og noen eksempler:
1. Halogenering med alkaner: Siden alkaner er dårlig reaktive, skjer halogeneringsreaksjonene bare i nærvær av sollys (λ), ultrafiolett lys eller sterk oppvarming. Denne typen reaksjon gjøres for å få et alkylhalogenid.
Eksempel: metanmonoklorering:
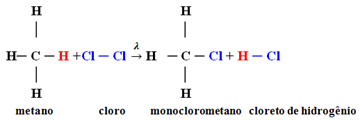
I dette tilfellet skjedde det fra et hydrogenatom av metan (CH
4) erstattes av et kloratom som gir monoklormetan. Hvis det var for mye klor, kunne denne reaksjonen fortsette å prosessere, og erstatte alle hydrogenene i metanet.1.1. Halogenering i alkaner med mer enn 3 karbonatomer: Hvis alkanen som skal reageres har minst 3 karbonatomer, ender vi opp med en blanding av forskjellige substituerte forbindelser. Se eksemplet nedenfor for en metylbutanmonoklorinering:
Ikke stopp nå... Det er mer etter annonseringen;)
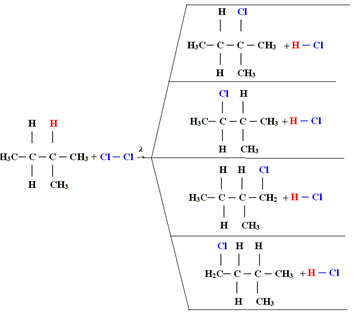
Mengden av hver forbindelse vil være proporsjonal med følgende rekkefølge hvor lett hydrogen frigjøres i molekylet:

I tilfelle ovenfor vil således den største mengden være 2-metyl-2-klorbutan og den minste mengde vil være 2-metyl-1-klorbutan.
2. Benzenhalogenering: Benzen reagerer normalt ikke med klor eller brom. Imidlertid, hvis en Lewis-syre brukes som katalysator (vanligvis brukes FeCl3, FeBr3 eller AlCl3, alt i vannfri form), reagerer benzen lett i en halogeneringsreaksjon.
Kloridet og jernbromidet kan oppnås ved å bare tilsette jern til blandingen, og på denne måten reagerer det med halogenet og produserer Lewis-syren:
2 Fe + 3 Br2 → 2 FeBr3
Se et eksempel på benzenhalogenering og dens mekanisme:
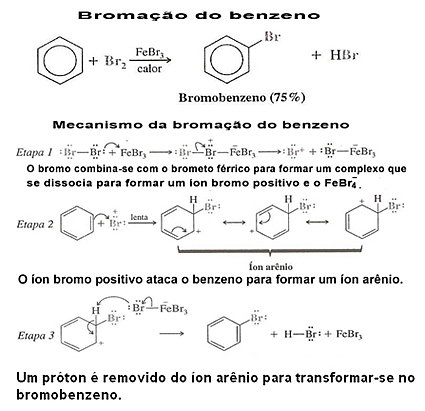
3. Halogenering av benzenderivater:I slike tilfeller styres substitusjonen av substituenten eller den funksjonelle gruppen som er festet til den aromatiske kjernen. For å se hvordan dette skjer, les tekstene "Styringsradikaler i benzenringen"og"Elektroniske effekter av meta og orto-til-regissører radikaler”.
Av Jennifer Fogaça
Uteksamen i kjemi
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Organiske halogeneringsreaksjoner"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm. Tilgang 28. juni 2021.