Noen forbindelser trenger ikke å ha åtte elektroner i valensskallet for å oppnå stabilitet, så de regnes som unntak fra oktetregelen. Lær nå hvorfor noen elementer slipper plikten til å ha en oktett elektroner i det siste skallet.
Beryllium (Være)
Det er et unntak fra oktetregelen fordi den er i stand til å danne forbindelser med to enkeltbindinger, så den stabiliserer seg med bare fire elektroner i valensskallet. 
Siden hydrogen (H) må gi opp to elektroner for å lage bindingen (H - Vel - H), deler Beryllium (Be) -atomet sine elektroner og oppnår stabilitet.
Aluminium (Al)
Det er et unntak fra Octet-regelen fordi det oppnår stabilitet med seks elektroner i valensskallet. Aluminiumatomet har en tendens til å donere elektronene sine og kan danne tre enkeltbindinger med andre atomer: 
I dette tilfellet dannet aluminium (Al) tre bindinger med tre fluor (F) -atomer.
Bor (B)
Det danner molekylære stoffer med tre enkeltbindinger. 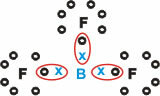
Merk at Bor (B) har en tendens til å donere elektronene til fluor (F) -atomer, som adlyder oktetregelen, og krever åtte elektroner i valensskallet. Når bor gir opp elektronene, stabiliserer fluor seg med den dannede oktetten.
Av Líria Alves
Uteksamen i kjemi
Brasil skolelag
Se mer!
Oktettteori
Generell kjemi - Kjemi - Brasilskolen
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm


