Osmose er en kolligativ egenskap konseptualisert som passering av løsemiddel gjennom semipermeable membraner. Derav betydningen av den greske opprinnelsen til navnet sitt: osmos = impuls. I denne prosessen er det en diffusjon av løsningsmiddel fra den mindre konsentrerte (eller mer fortynnede) løsningen til den mer konsentrerte (mindre fortynnede), og tilsvarer dermed konsentrasjonen av begge løsningene.
Imidlertid, spesielt i kystregioner, som har lite drikkevann, brukes en teknikk for å transformere saltvann til ferskvann, det vil si i motsatt retning av den beskrevne osmosen. Derfor kalles det omvendt osmose eller omvendt osmose (eller omvendt osmose). I denne prosessen passerer løsningsmidlet gjennom den semipermeable membranen fra den mest konsentrerte løsningen til den minst konsentrerte løsningen.
Med dette målet om avsaltning av sjøvann er det bygd mange planter, som den i Yuma i Arizona (USA), som har kapasitet til å produsere 72 millioner liter rent vann per dag. I 2010 ble det største avsaltingsanlegget i verden innviet i Israel. Bygget for å produsere 127 millioner kubikkmeter vann i året - nok til å levere en sjettedel av den israelske befolkningen.
I Brasil er eksempler de greske øyene, øyene Fernando de Noronha, Påskeøya og øya Malta. I tillegg til å bruke denne prosessen i brakkvann (som kommer fra undergrunnen, som inneholder mye salt) i visse regioner i det nordøstlige Brasil.
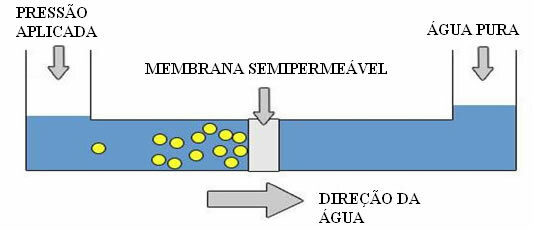
Men hvordan er dette mulig? Dette skyldes det osmotiske trykket, det vil si det ytre trykket som påføres løsningen, for å forhindre innføring av rent vann. Hvis dette trykket økes kraftig, oppnås omvendt osmose der det passerer vann fra løsningen til rent vann.
Omvendt osmoseordning
Av Jennifer Fogaça
Uteksamen i kjemi
Brasil skolelag
Fysisk-kjemisk - Kjemi - Brasilskolen
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/osmose-reversa-na-dessalinizacao-das-aguas-dos-mares.htm