Kp er akronymet som brukes for å bestemme konstant for en likevekt når det gjelder deltrykk. Denne konstanten fungerer med verdiene til de gassformige deltakerne i en likevekt i atm-enheten, for eksempel.

Ligning som representerer en kjemisk reaksjon med gassformige komponenter
I denne ligningen er alle deltakerne gassformede, så når en deltakende gass har en partialtrykk i blandingen, er det representert med forkortelsen pX.
Når du setter opp den kjemiske likevektsligningen (i form av konsentrasjon), må produktene plasseres i telleren og reaktantene plasseres i nevneren:
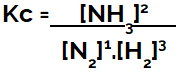
Kc uttrykk for ammoniakkformasjonslikevekt
uttrykket for likevektskonstant i form av trykk (Kp) følger mønsteret til Kc, det vil si at partialtrykket til reagensene er plassert i nevneren og partialtrykket til produktene i telleren:
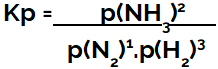
Kp uttrykk for ammoniakkformasjonslikevekt
Observasjon: Hvis reaksjonsligningen til kjemisk balanse ikke presentere noen gassformig deltaker, vil den ikke automatisk presentere Kp.
Eksempel: (PUC-MG)
For reaksjonen: 2 CO(g) + O2(g)? 2 CO2(g), partialtrykket til CO(g) det er2(g) ved likevekt er de henholdsvis 0,2 atm og 0,4 atm. Det totale systemtrykket er 1,4 atm. Verdien av Kp for reaksjonen er:Ikke stopp nå... Det er mer etter reklamen ;)
a) 56,2
b) 40,0
c) 35,6
d) 28.4
e) 25.6
Dataene gitt av øvelsen er:
Karbonmonoksid partialtrykk (pCO) = 0,2 atm;
Partialtrykk av karbonmonoksid (pO2) = 0,4 atm;
Totalt trykk =1,4 atm;
For å bestemme Kp til dette systemet, må vi utføre følgende trinn:
1. trinn: Bestem partialtrykket til karbonmonoksid (pCO2).
For dette, bare husk at det totale trykket (pt) er summen av alle partialtrykk:
pt = pCO + pCO2 + pO2
1,4 = 0,2 + p (CO2) + 0,4
1,4 - 0,2 - 0,4 = pCO2
pCO2 = 0,8 atm
2. trinn: Bestem Kp for øvelsen.
For dette, bruk bare verdiene i uttrykket for likevektskonstanten Kp:
Kp = (pCO2)2
(pCO)2.(støv2)1
Kp = (0,8)2
(0,2)2.(0,4)1
Kp = 0,64
0,04.0,4
Kp = 0,64
0,016
Kp = 40 atm-1
Av meg Diogo Lopes Dias
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
DAGER, Diogo Lopes. "Hva er Kp?"; Brasil skole. Tilgjengelig i: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kp.htm. Åpnet 27. juli 2021.


