O ligningsbalansering lar oss matche antallet atomer som er til stede i den kjemiske ligningen, slik at den blir sant og representerer en kjemisk reaksjon.
Bruk spørsmålene nedenfor for å teste kunnskapen din og sjekk svarene som er kommentert etter tilbakemeldingen for å svare på spørsmålene dine.
Spørsmål 1
(Mackenzie-SP)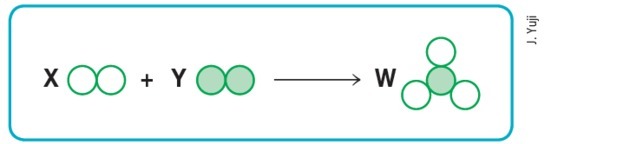
Forutsatt at henholdsvis de tomme og fylte sirkler betyr forskjellige atomer, er ordningen ovenfor vil representere en balansert kjemisk reaksjon hvis vi erstatter henholdsvis bokstavene X, Y og W med verdier:
a) 1, 2 og 3.
b) 1, 2 og 2.
c) 2, 1 og 3.
d) 3, 1 og 2.
e) 3, 2 og 2.
Alternativ d) 3, 1 og 2.
Første trinn: Vi tilordner bokstaver for å gjøre ligningen lettere å forstå.
2. trinn: vi legger sammen indeksene for å finne ut hvem som har flest atomer i ligningen.
| DE | |
| B |
A og B vises bare en gang i hvert medlem av ligningen. Men hvis vi legger til indeksene, ser vi at A har den høyeste verdien. Derfor startet vi balanseringen for ham.
Tredje trinn: Vi balanserer element A ved å transponere indeksene og gjøre dem om til koeffisienter.
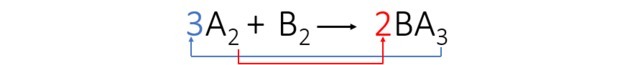
Vi observerte at element B automatisk ble balansert og koeffisientene til ligningen er: 3, 1 og 2.
spørsmål 2
(Unicamp-SP) Les følgende setning og transformer den til en (balansert) kjemisk ligning, ved hjelp av symboler og formler: “et molekyl av gassformig nitrogen, som inneholder to atomer av nitrogen per molekyl, reagerer med tre molekyler av diatomisk, gassformig hydrogen, og produserer to molekyler av gassformig ammoniakk, som består av tre hydrogenatomer og en av nitrogen ".
Svare:
Når vi representerer atomene som er beskrevet i spørsmålet, kan vi forstå at reaksjonen skjer som følger:
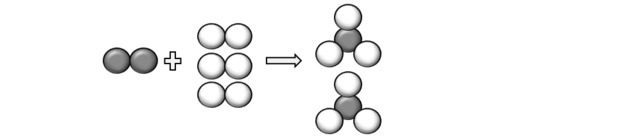
Så vi kommer til ligningen:
spørsmål 3
Hydrogenperoksid er en kjemisk forbindelse som kan spaltes og danne vann og oksygen, i henhold til den kjemiske ligningen nedenfor.
Når det gjelder denne reaksjonen, er den riktig balanserte ligningen:
a) H2O2 →2 + H2O
b) 2t2O2 →2 + 2H2O
c) H2O2 → 2O2 + H2O
d) 2t2O2 → 2O2 + 2H2O
Riktig alternativ: b) 2H2O2 →2 + 2H2O
Merk at hydrogenperoksid er et kjemikalie som består av atomer av to kjemiske grunnstoffer: hydrogen og oksygen.
Etter nedbrytningsreaksjonen må du ha samme antall atomer av de to elementene i både reaktantene og produktene. For dette må vi balansere ligningen.
Merk at vi har 2 hydrogenatomer i reaktanten (H2O2) og to atomer i produktet (H2O). Imidlertid har oksygen to atomer i reaktanten (H2O2) og tre atomer i produktene (H2O og O2).
Hvis vi setter koeffisienten 2 foran hydrogenperoksidet, dobler vi antall atomene til elementene.
Merk at hvis vi setter den samme koeffisienten sammen med formelen for vann, har vi samme mengde atomer på begge sider.
Derfor er den riktig balanserte kjemiske ligningen 2H2O2 →2 + 2H2O.
spørsmål 4
(UFPE) Vurder de kjemiske reaksjonene nedenfor.
Vi kan si det:
a) alle er balanserte.
b) 2, 3 og 4 er balansert.
c) bare 2 og 4 er balansert.
d) bare 1 er ubalansert.
e) ingen er riktig balansert, fordi de fysiske tilstandene til reaktantene og produktene er forskjellige.
Alternativ b) 2, 3 og 4 er balansert.
Alternativ 1 og 5 er feil fordi:
- Ligning 1 er ubalansert, den rette balansen vil være:
- Ligning 5 er feil fordi forbindelsen dannet i reaksjonen ville være H2KUN3.
Å danne H2KUN4 bør inkluderes i ligningen oksidasjonen av SO2.
spørsmål 5
(Mackenzie-SP) Oppvarmet til 800 ° C nedbrytes kalsiumkarbonat i kalsiumoksid (jomfru kalk) og karbondioksid. Den riktig balanserte ligningen, som tilsvarer det beskrevne fenomenet, er:
(Gitt: Ca - jordalkalimetall.)
Alternativ c)
Kalsium er et jordalkalimetall og for å ha stabilitet trenger kalsium 2 elektroner (Ca2+), som er oksygenladningen (O2-).
Dermed binder et kalsiumatom til et oksygenatom og forbindelsen som dannes er CaO, som er kalk.
Det andre produktet er karbondioksid (CO2). Begge er dannet av kalsiumkarbonat (CaCO3).
Sette det inn i en ligning:
Vi bemerker at mengdene av atomer allerede er riktige og ikke trenger balansering.
spørsmål 6
(UFMG) Ligningen er ikke balansert. Når du balanserer det med minst mulig tall, vil summen av de støkiometriske koeffisientene være:
a) 4
b) 7
c) 10
d) 11
e) 12
Alternativ e) 12
Ved å bruke prøvemetoden vil balanseringsordren være:
1. trinn: Ettersom elementet som bare vises en gang i hvert medlem og som har den høyeste indeksen, er kalsium, begynte vi å balansere for det.
2. trinn: Vi følger balanseringen av den radikale PO43-, som også bare vises en gang.
3. trinn: vi balanserer hydrogenet.
Med det observerer vi at mengden oksygen automatisk ble justert og balansen i ligningen er:
Husk at når koeffisienten er 1, trenger du ikke å skrive den i ligningen.
Legge til koeffisientene vi har:
spørsmål 7
Forbrenning er en type kjemisk reaksjon der energi frigjøres i form av varme.
Ved fullstendig forbrenning av et stoff dannet av karbon og hydrogen dannes karbondioksid og vann.
Observer hydrokarbonforbrenningsreaksjonene og svar på hvilken av ligningene nedenfor som er feil balansert:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 3O2 → 4CO2 + 5t2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Feil svar: c) C4H10 + 13 / 3O2 → 4CO2 + 5t2O
For å balansere de kjemiske ligningene, la oss først se på hvilket element som bare vises en gang i hvert medlem av ligningen.
Merk at karbon og hydrogen bare danner en reaktant og ett produkt i hver ligning som presenteres.
Så la oss begynne å balansere med hydrogen, ettersom det har et større antall atomer.
Derfor vil rekkefølgen på balansering være:
- Hydrogen
- Karbon
- Oksygen
Hydrogen
Ettersom produktet har 2 hydrogenatomer, setter vi inn et tall som en koeffisient som ganget med 2 resulterer i antall hydrogenatomer i reaktanten.
a) CH4 + O2 → CO2 + 2H2O
b) C3H8 + O2 → CO2 + 4H2O
c) C4H10 + O2 → CO2 + 5H2O
d) C2H6 + O2 → CO2 + 3H2O
Karbon
Balansering gjøres ved å transponere karbonindeksen i reaktanten og bruke den som en koeffisient på produktet som har atomer av dette elementet.
a) CH4 + O2 → 1CO2 + 2H2O
b) C3H8 + O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5t2O
d) C2H6 + O2 → 2CO2 + 3H2O
Oksygen
Når vi legger til antall oksygenatomer i de dannede produktene, finner vi antall atomer i elementet som må reagere.
For det må vi sette som koeffisient et tall som multiplisert med 2 resulterer i antall oksygenatomer i produktene.
a) CH4 + O2 → 1CO2 + 2H2O
2x = 2 + 2
2x = 4
x = 2
Så den riktige ligningen er: CH4 + 2O2 → 1CO2 + 2H2O.
b) C3H8 + O2 → 3CO2 + 4H2O
2x = 6 + 4
2x = 10
x = 5
Så den riktige ligningen er: C3H8 + 5O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5t2O
2x = 8 + 5
2x = 13
x = 13/2
Så den riktige ligningen er: C4H10 + 13/2O2 → 4CO2+ 5t2O
d) C2H6 + O2 → 2CO2 + 3H2O
2x = 4 + 3
2x = 7
x = 7/2
Så den riktige ligningen er: C2H6 + 7/2O2 → 2CO2 + 3H2O
Korrekt balanserte ligninger er:
a) CH4 + 2O2 → CO2 + 2H2O
b) C3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 2O2 → 4CO2 + 5t2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Dermed alternativ c) C4H10 + 13 / 3O2 → 4CO2 + 5t2Saken er at den ikke har riktig balanse.
spørsmål 8
(Enem 2015) Kalkstein er materialer sammensatt av kalsiumkarbonat, som kan fungere som sorbenter for svoveldioksid (SO2), et viktig luftforurensende stoff. Reaksjonene involvert i prosessen er aktivering av kalkstein, gjennom kalsinering, og fiksering av SO2 med dannelsen av et kalsiumsalt, som illustrert av de forenklede kjemiske ligningene.
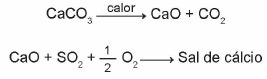
Med tanke på reaksjonene som er involvert i denne avsvovlingsprosessen, tilsvarer den kjemiske formelen til kalsiumsaltet:
Alternativ b)
Ettersom reaksjonen er balansert, må atomene i reaktantene være i samme mengde i produktene. Og dermed,
Saltet som dannes består av:
1 kalsiumatom = Ca
1 svovelatom = S
4 oksygenatomer = O4
Derfor tilsvarer den kjemiske formelen til kalsiumsalt CaSO4.
spørsmål 9
(UFPI) Reaksjonen av X med Y er vist nedenfor. Bestem hvilken ligning som best representerer den balanserte kjemiske ligningen.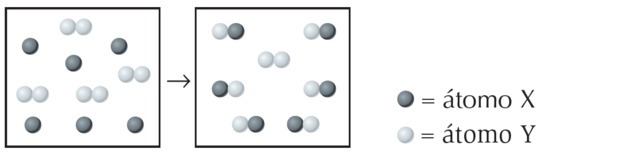
Alternativ a)
I figuren observerer vi at arten X er et enkelt atom mens Y er diatomisk, det vil si at den dannes ved sammenføyning av 2 atomer. Så X reagerer med Y2.
Det dannede produktet er representert av XY, ligningen er ubalansert:
Vi balanserer ligningen som følger:
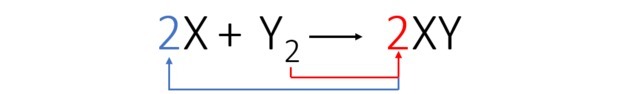
I henhold til den balanserte ligningen viser figuren oss hvordan reaksjonen oppstår og dens andel.
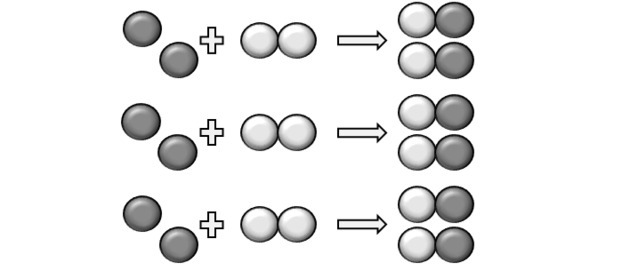
For at en reaksjon skal skje, må det være et fast forhold, og det kan derfor hende at en eller annen forbindelse ikke reagerer. Dette er hva figuren viser, for i produktet ser vi at en Y2 reagerte ikke.
spørsmål 10
(Enem 2010) Mobiliseringer for å fremme en bedre planet for fremtidige generasjoner er stadig hyppigere. De fleste transportmidler drives for tiden ved å brenne et fossilt drivstoff. Som et eksempel på belastningen som denne fremgangsmåten medfører, er det nok å vite at en bil i gjennomsnitt produserer omtrent 200 g karbondioksid per tilbakelagt km.
Global Warming Magazine. År 2, 8. Publisering av Instituto Brasileiro de Cultura Ltda.
En av hovedbestanddelene av bensin er oktan (C8H18). Gjennom forbrenning av oktan er energi mulig, slik at bilen kan begynne å bevege seg. Ligningen som representerer den kjemiske reaksjonen i denne prosessen viser at:
a) oksygen frigjøres i prosessen, i form av O2.
b) den støkiometriske koeffisienten for vann er 8 til 1 oktan.
c) i prosessen er det vannforbruk, slik at energi frigjøres.
d) den støkiometriske koeffisienten for oksygen er 12,5 til 1 oktan.
e) den støkiometriske koeffisienten for karbondioksid er 9 til 1 oktan
Alternativ d) den støkiometriske koeffisienten for oksygen er 12,5 til 1 oktan.
Når vi balanserer ligningen, finner vi følgende koeffisienter:
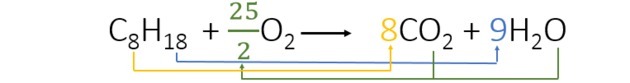
- Vi startet balanseringen av hydrogen som bare vises en gang i hvert medlem og har en høyere indeks. Siden det er 18 reagerende hydrogenatomer, er det 2 i produktet, så vi må legge til et tall multiplisert med 2 gir 18. Så 9 er koeffisienten.
- Deretter legger vi til koeffisienten 8 foran CO2 å ha 8 karbonatomer i hvert medlem av ligningen.
- Til slutt er det bare å legge til mengden oksygen i produktet og finne verdien som multiplisert med 2 gir oss 25 oksygenatomer. Så vi valgte 25/2 eller 12.5.
For forbrenning av 1 oktan forbrukes 12,5 oksygen.
spørsmål 11
(Fatec-SP) En viktig egenskap ved gjødsel er deres vannløselighet. Gjødselindustrien forvandler derfor kalsiumfosfat, hvis løselighet i vann er veldig lav, til en mye mer løselig forbindelse, som er kalsiumsulfosfat. Denne prosessen er representert ved ligningen:
hvor verdiene av henholdsvis x, y og z er:
a) 4, 2 og 2.
b) 3, 6 og 3.
c) 2, 2 og 2.
d) 5, 2 og 3.
e) 3, 2 og 2.
Alternativ e) 3, 2 og 2.
Ved å bruke den algebraiske metoden danner vi ligninger for hvert element og likestiller antall atomer i reaktanten med antall atomer i produktet. Derfor:
Balansert ligning:
spørsmål 12
Balansere ligningene nedenfor ved hjelp av prøvemetoden.
Svare:
Ligningen består av grunnstoffene hydrogen og klor. Vi balanserer elementene bare ved å legge til koeffisient 2 foran produktet.
Ligningen trengte ikke balanseres, ettersom atommengdene allerede er justert.
Fosfor har to atomer i reaktantene, så for å balansere dette elementet justerer vi mengden fosforsyre i produktet til 2H3STØV4.
Etter det observerte vi at hydrogenet hadde 6 atomer i produktet, vi balanserte mengden av dette elementet og tilførte koeffisient 3 til reaktanten som inneholder den.
Med de foregående trinnene ble mengden oksygen korrigert.
Ser vi på ligningen ser vi at mengdene hydrogen og brom i produktene er dobbelt så høye hvis det er i reagensene, så legger vi koeffisient 2 til HBr for å balansere disse to elementer.
Klor har 3 atomer i produktene og bare 1 i reaktantene, så vi balanserer å sette en koeffisient på 3 foran HCl.
Hydrogenet hadde 3 atomer i reaktantene og 2 atomer i produktene. For å justere mengdene transformerer vi H-indeksen2 i koeffisient multipliserer vi med 3 som allerede var i HC1 og får resultatet av 6 HCI.
Vi justerer mengden klor i produktene for også å ha 6 atomer og få 2AlCl3.
Aluminium hadde 2 atomer i produktene, vi justerte mengden i reaktantene til 2Al.
Vi balanserer mengden hydrogen i produktet til 3H2 og vi tilpasser mengden på 6 atomer av det elementet i hvert begrep i ligningen.
I ligningen er nitratradikalet (NO3-) har indeks 2 i produktet, transformerer vi indeksen til koeffisient i reaktanten for 2AgNO3.
Mengden sølv måtte justeres, siden den nå har 2 atomer i reagensene, så vi har 2Ag i produktet.
I reaktantene har vi 4 hydrogenatomer, og for å balansere dette elementet legger vi koeffisient 2 til HCl-produktet.
Klor har nå 4 atomer i produktene, så vi justerer mengden i reagenset til 2Cl2.
Vi har 6 hydrogenatomer i reaktantene, og for å balansere dette elementet justerer vi vannmengden til 3H2O.
Vi har 2 karbonatomer i reaktantene, og for å balansere dette elementet justerer vi mengden karbondioksid til 2CO2.
Oksygen må ha 7 atomer i reaktantene, og for å balansere dette elementet justerer vi mengden molekylært oksygen til 3O2.
Ser vi på ligningen, nitratradikalen (NO3-) har indeks 2 i produktet. Vi forvandler indeksen til koeffisient 2 i AgNO-reagenset3.
Vi har 2 sølvatomer i reaktantene, og for å balansere dette elementet justerer vi mengden sølvklorid i produktet til 2AgCl.
Vi har 3 kalsiumatomer i produktet, og for å balansere dette elementet justerer vi mengden kalsiumnitrat i reagenset til 3Ca (NO3)2.
Vi sitter da igjen med 6 NO-radikaler3- i reaktantene og for å balansere dette radikale justerer vi mengden salpetersyre i produktene til 6HNO3.
Vi har nå 6 hydrogenatomer i produktene, og for å balansere dette elementet justerer vi mengden fosforsyre i reagenset til 2H3STØV4.
Lær mer om beregninger med kjemiske ligninger på:
- Balansere kjemiske ligninger
- Støkiometri
- Støkiometriske beregninger
- Støkiometriøvelser
- Periodiske øvelser