Som forklart i teksten “Katalyse og katalysator”, Katalysatorer er kjemiske arter som akselererer reaksjonshastigheten. Bruken er veldig nyttig i kjemisk industri, der det søkes å spare så mye tid som mulig i produksjonen.
I visse situasjoner er det imidlertid mer interessant at reaksjonen går saktere; som for eksempel når du vil bestemme hastigheten på veldig raske reaksjoner. For å oppnå denne prestasjonen, kontrollere og studere disse reaksjonene, er det vanlig å legge til et stoff som bremser reaksjonene, som kalles hemmere, giftstoffer eller antikatalysatorer.
Disse kjemiske artene kombineres med katalysatoren, noe som opphever eller reduserer dens virkning. Dette er mulig fordi katalysatorens virkningsmekanisme er å redusere aktiveringsenergien, forenkle reaksjonsprosessen og øke hastigheten; allerede hemmere virker omvendt, noe som betyr at de øker aktiveringsenergien som trengs for at reaktantene skal nå det aktiverte komplekset.
Et eksempel som kan nevnes er arsen (As), som har denne funksjonen i Haber-Bosch-reaksjonen, en reaksjon som er mye brukt i industrien for produksjon av ammoniakk, ved bruk av jern (Fe
(s)) som katalysator. Dermed blir effektiviteten til jern veldig liten i nærvær av arsen, som hemmer det, det vil si det er katalysatorgiften til denne reaksjonen, som er vist nedenfor: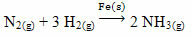
Arsen kan også utøve en antikatalytisk virkning når man bruker metallisk platina (Pt(s)) som en katalysator for SO-forbrenningsreaksjonen2 (g), for produksjon av svoveltrioksid (SO3 (g)). Tilstedeværelsen av arsen, selv i små mengder, avbryter den katalytiske virkningen av platina, noe som kan lamme en del av produksjonen. Derfor brukes divanadiumpentoksid normalt i bransjer som håndterer denne produksjonen (V2O5 (s)) som en katalysator i stedet for platina.
Ikke stopp nå... Det er mer etter annonseringen;)
Et annet eksempel forekommer i følgende hydrogenperoksydnedbrytningsreaksjon:
2 timer2O2 (aq) → 2 H2O(1) + 1 O2 (g)
I dette tilfellet er en hemmer som kan brukes noe syre, fordi når mediet er surt, fortsetter reaksjonen saktere.
Men inhibitoren er også mye brukt av industrien, hovedsakelig for å fungere som en reaksjonshemmer for naturlig nedbrytning av mat, drikke, kosmetikk og medisiner.
Kosmetikk kan for eksempel ta lang tid å nå forbrukeren; således brukes forskjellige konserveringsmidler i dem, slik som propylparaben, som brukes i oljefasen og fungerer som et soppdrepende middel, og metylparaben, som brukes i den vandige fasen og som har en antiseptisk effekt. Deres respektive strukturer er vist nedenfor:
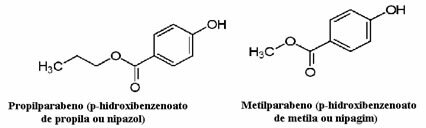
Det er interessant at på mange kosmetiske etiketter er det følgende setning: "Det inneholder ikke parabener". Dette betyr at denne kosmetikken ikke har disse konserveringsmidlene som vi nevnte, og at de normalt ikke er testet på dyr.
Av Jennifer Fogaça
Uteksamen i kjemi
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Katalysatorinhibitorer"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/inibidores-catalisador.htm. Tilgang 27. juni 2021.