Ordet "gass" ble først brukt av forskeren Van Helmont (1577-1644), som kom fra gresk kaos, det vil si “kaos”, fordi molekylene eller atomer oppfører seg på en uordnet måte.
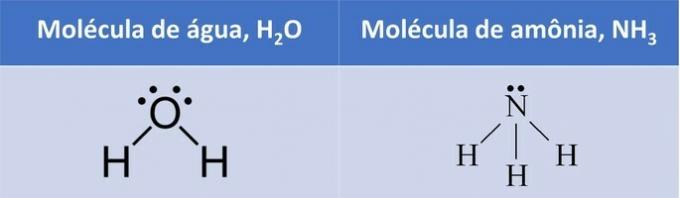
Gasser er molekylære forbindelser eller i form av isolerte atomer (edelgasser) med spesifikke egenskaper, inkludert, vi kan markere at de ikke har et definert volum eller form, og har en tendens til å oppta volumet og holde seg i form av beholderen som inneholder.
Volum, trykk og temperatur er de grunnleggende størrelsene som må tas i betraktning i studien av gasser, som kalles gasstilstandsvariabler.
Denne studien er veldig viktig både fra et teoretisk og et praktisk synspunkt. For eksempel var det gjennom å forstå gassens atferd at kjemiske reaksjoner ble forstått best. I tillegg er stoffer i gassform overalt, som deltar i viktige prosesser i vedlikehold av livet: luften vi puster inn er en gassformig blanding som hovedsakelig består av nitrogen og oksygen; oksygengass brukes på sykehus, stålfabrikker, metallskjærings- og sveisebrennere; vi bruker gassene til matlaging, for å flytte kjøretøy, for å blåse opp ballonger og så videre.
Ikke stopp nå... Det er mer etter annonseringen;)
Disse og andre prosesser som involverer gasser vil bli dekket i artiklene i denne kjemi-delen.
Av Jennifer Fogaça
Uteksamen i kjemi
(UnB-DF) Studien av gassers makroskopiske egenskaper tillot utvikling av den kinetisk-molekylære teorien, som på mikroskopisk nivå forklarer gassers oppførsel. Når det gjelder denne teorien, må du bedømme følgende punkter:
(1) Gassens oppførsel er relatert til den ensartede og ordnede bevegelsen av molekylene deres.
(3) Ideelle gasser eksisterer ikke, da de kun er teoretiske modeller der volumet av molekyler og deres interaksjoner anses å være ubetydelige.
(4) Trykket til en gass inne i en beholder er assosiert med kollisjoner av gassmolekyler med veggene i beholderen.
JEG. Trykket fra en gass er resultatet av at molekylene kolliderer med beholderens vegger.
II. Den gjennomsnittlige kinetiske energien til molekylene til en gass er direkte proporsjonal med den absolutte temperaturen.
III. Volum, trykk og temperatur kalles tilstandsvariabler.
IV. Molekylene beveger seg uten å kollidere med veggene i beholderen som inneholder dem.