Atomiske modeller kom fram av behovet for å forklare strukturen til atomer. Da nye bevis på konstitusjonen av atomer ble presentert, prøvde en ny atommodell å avklare funnene.
De greske filosofene Democritus og Leucipo i V-tallet; Ç. kalt atomet, fra gresk ατoμoν, den udelelige partikkelen og den minste delen av materien.
Selv om atombegrepet er gammelt, går utviklingen av atomteorier tilbake til det 19. og 20. århundre. Derfor var de viktigste atommodellene som ble utviklet for å forstå materiens natur:
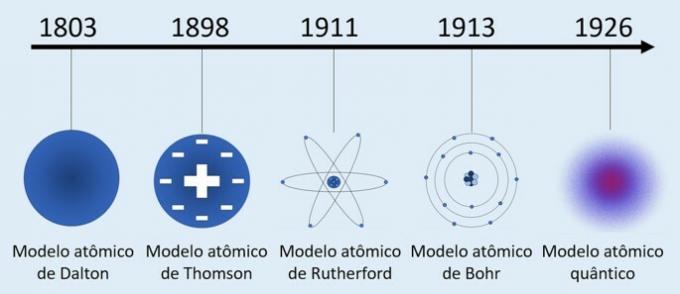
- Daltons Atomic Model (1803) - "Billiard Ball Model"
- Thomson Atomic Model (1898) - "Rain Pudding Model"
- Rutherfords Atomic Model (1911) - "Nuclear Model"
- Bohrs Atomic Model (1913) - "Planetary Model"
- Quantum Atomic Model (1926) - "Electronic Cloud Model"
Daltons atommodell
Det første anerkjente forsøket på å beskrive atomer kom fra den engelske forskeren John Dalton (1766-1844) i en modell som ble populært kjent som "biljardkulen".
Dalton's Atom (1803): massiv, udelelig og uforgjengelig sfære.

I følge Dalton:
- Alle stoffer dannes av atomer;
- Atomene til et kjemisk element er identiske i størrelse og egenskaper, mens de til forskjellige kjemiske elementer er forskjellige;
- Stoffer er resultatet av en kjemisk reaksjon, som består av rekombinasjon av atomer.
Negative poeng: Siden elektroner ennå ikke var kjent da Dalton formulerte sin teori, ble disse partiklene, som vi nå vet å være en del av atomer, ikke vurdert.
Lære mer om Daltons atommodell.
Thomson Atomic Model
Joseph John Thomson (1856-1940) var ansvarlig for å oppdage eksistensen av elektroner, partikler utstyrt med en negativ ladning og som er en del av atomer. Denne oppdagelsen veltet Daltons atomteori om at atomet er udelelig, men dannet av enda mindre partikler, og derfor ble det kjent som “rosinpudding”.
Thomson's Atom (1898): positivt ladet kule med faste elektroner.

Ifølge Thomson:
- Atomet er elektrisk nøytralt;
- Elektroner fester seg til en positivt ladet overflate;
- Det er en frastøting mellom elektroner fordelt i atomer.
Negative poeng: Selv om Thomson tok hensyn til eksistensen av elektroner, er atomet ikke en positiv sfære, men heller utstyrt med positivt ladede partikler, protonene, identifisert i 1886 av forskeren Eugene Goldstein og senere bekreftet av Ernest Rutherford.
Lære mer om Thomson atommodell.
Rutherford Atomic Model
Gjennom eksperimentene klarte Ernest Rutherford (1871-1937) å demonstrere at atomet ikke var en udelelig partikkel som antatt, men at det ble dannet av mindre partikler.
Rutherford's Atom (1911): positivt ladet kjerne og elektroner er plassert rundt den i elektrosfæren.
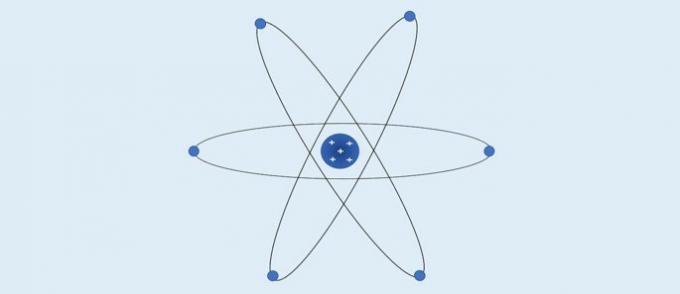
I følge Rutherford:
- Atomet har en sentral region med høy konsentrasjon av positiv ladning;
- Massen til et atom er konsentrert i sin sentrale region;
- Elektroner er lettere og ligger rundt kjernen, en region som inneholder mange tomme rom.
Negative punkter: Atomkjernen har ikke bare positivt ladede partikler, men det er også andre subatomære partikler, nøytronene, oppdaget av James Chadwick i 1932. Videre forklarte ikke modellen som ble foreslått av Rutherford ikke utslipp av lys fra atomer.
Lære mer om Rutherford atommodell.
Bohrs atommodell
Søker å forklare hvorfor elementene avgir karakteristiske farger når de utsettes for noen forhold og basert på Rutherfords atommodell, Niels Bohr (1885-1962), foreslo en atomteori som forklarte utslipp av lys i visse frekvenser.
Bohrs Atom (1913): elektroner beveger seg i faste sirkulære lag rundt kjernen.
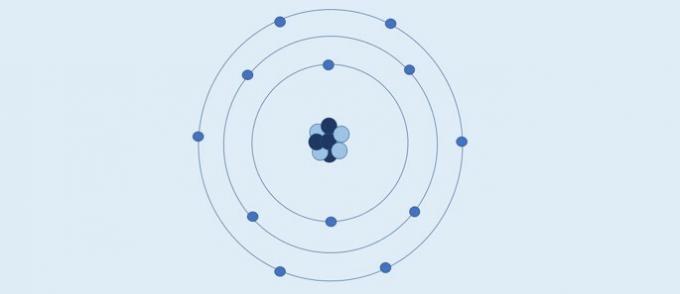
I følge Bohr:
- Elektroner beveger seg i lagene rundt kjernen;
- Lagene rundt kjernen har spesifikke energiverdier;
- For å gå til et mer eksternt nivå, må elektronen absorbere energi. Ved retur til et lag nærmere kjernen frigjør elektronen energi.
Negative poeng: Det kan ikke sies at elektroner beveger seg rundt kjernen i faste posisjoner som planeter rundt solen.
Lære mer om Bohr atommodell.
Quantum Atomic Model
Mange forskere har bidratt til utviklingen av kvantemekanikk, som prøver å forklare den "mer reelle" strukturen til en atom ved kombinasjonen av flere studier, og derfor er det den mest komplekse.
Quantum Atom (1926): kjernen består av protoner (positiv ladning) og nøytroner (nullladning), og elektroner (negativ ladning) danner en elektronisk sky rundt kjernen.
I henhold til kvanteatommodellen:
- Kjernen består av protoner og nøytroner. Siden bare protoner har en ladning, er kjernen positivt ladet;
- Elektroner danner en elektronisk sky rundt kjernen;
- Elektroner beveger seg i orbitaler, i et tredimensjonalt rom;
- Den nøyaktige plasseringen av et elektron kan ikke defineres. Det som gjøres er beregninger som bestemmer sannsynligheten for at et elektron vil være i en gitt tid.
Du kvantetall har funksjonen til å lokalisere elektronene. Er de:
O hovedkvantetall (n) representerer energinivåene, det vil si de elektroniske lagene til et atom.
O sekundært kvantetall (l) angir energinivåene, det vil si energinivånivået som elektronet tilhører.
O magnetisk kvantetall (m) er den som indikerer banen der elektronene møtes.
Lære mer om atommodeller og test din kunnskap med øvelser på atommodeller.