그만큼 반응 속도의 법칙 물질의 양 (mol / L)에서 시약의 농도와 화학적 변환의 속도를 연결하며 다음과 같이 나타낼 수 있습니다.

예를 들어 다음과 같은 일반적인 반응을 고려하십시오.
aA + bB → cC + dD
반응물 A와 B의 농도를 높이면 반응 속도는 어떻게됩니까? 글쎄요, 같은 공간에서 반응물 입자의 양이 증가함에 따라 그들 사이에 더 효과적인 충돌이 일어나 반응 발달 속도가 증가 할 것입니다. 즉, 속도가 빨라집니다.
따라서 반응 속도는 반응물의 농도에 정비례합니다. 그러나 온도에 따라 다릅니다. 따라서 반응 속도의 법칙을 나타내는 다음과 같은 수학 방정식이 있습니다.

에 무슨:
v = 반응 속도;
k = 온도 값에만 의존하는 상수;
α 및 β = 실험적으로 결정된 지수.
반응이 기본, 즉 단일 단계에서 발생하는 경우에만 지수가 균형 화학 방정식의 계수와 정확히 동일합니다. v = k. [그만큼]그만큼. [비]비. 그러나 다른 경우에는 각 시약의 농도를 높여야하는 적절한 효능을 실험적으로 결정해야합니다.
반응 속도의 법칙은 여러 이름으로 사용되며 다음과 같습니다. 매스 액션의 법칙, 속도 방정식, 반응의 운동 법칙 및 굴드 버그-웨이지 법칙.
이 법을 적용하는 방법의 예를 고려하십시오.
다음 기본 반응을 고려하십시오.
2 염산 (지) → 에이2(g) + Cl2(g)
a)이 반응의 속도에 대한 방정식을 쓰십시오.
b) 실험을 통해 25 ° C의 일정한 온도에서이 염화수소 가스 분해 반응의 속도와이 시약의 농도를 아래 표에 기록했습니다.
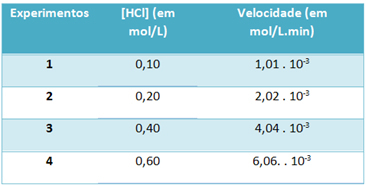
이를 바탕으로 언급 된 온도에서이 반응의 특성 속도 상수를 결정합니다.
해결:
그만큼) v = k. [HCl]2
b) v = k. [HCl]2
k = __V___
[HCl]2
k = 1,01. 10-3 몰. 엘-1. 분-1
0.01 mol. 엘-1
k = 1.01. 10-1 분-1
문자 "b"를 풀기 위해 얻은 값이 동일하다는 실험 데이터를 사용할 수 있습니다.
하지만 반응이 초보적이지 않다면 어떨까요? 비 초등 적 반응에서 이러한 질문을 어떻게 해결할 수 있습니까? 방법을 알아 보려면 비 기본 반응에 대한 속도 법칙을 읽어보십시오.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm

