კარბონატები არის არაორგანული ნაერთები, რომლებიც წარმოიქმნება ლითონის ან ნახევარგამტონის იონური კავშირით კარბონატულ ანიონთან, CO32-.
ნახშირბადი არის ტეტრავალენტური, ანუ მას აქვს ოთხი ელექტრონი ვალენტურ გარსში და მას შეუძლია შექმნას ოთხი კოვალენტური ბმა, რომ იყოს სტაბილური, ხოლო ჟანგბადი ორვალენტიანია, რომელსაც აქვს ექვსი ელექტრონი ვალენტურ გარსში და შეუძლია ორი ბმის შექმნა, რომ იყოს სტაბილური, რვა ელექტრონები. ამრიგად, ნახშირბადის ძლიერი მიდრეკილებაა ჟანგბადის ორ ატომთან, რაც სტაბილურია (O ═ C ═ O → კომპანია2).
მაგრამ სხვა ჟანგბადს შეუძლია შეუთავსოს ნახშირბადს, რადგან იონური სხივების თანაფარდობა კოორდინაციის რიცხვს უდრის 3 – ს, ქმნის სტრუქტურას სამკუთხა, რომელშიც ნახშირბადი ცენტრშია, ქმნის ორმაგ ბმას ჟანგბადის ერთ ატომთან და ორი ერთჯერადი ბმა დანარჩენ ორთან ჟანგბადები. შედეგი არის ორი ზედმეტი ელექტრონი, რადგან ეს ორი ჟანგბადი არ არის სტაბილური, საჭიროა თითო თითო ელექტრონის მიღება:
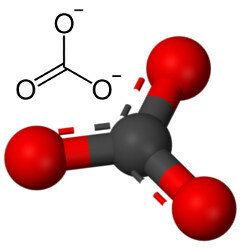
კარბონატული ანიონი იქმნება კოვალენტური ბმებით, მაგრამ მისი ნაერთები, რომლებიც არაორგანული მარილები და მინერალებია კარბონატების სახელით ცნობილია, რომ არის იონური, რადგან ეს რადიკალი იღებს ორ ელექტრონს ზოგიერთი ლითონისგან ან ნახევარგამტარიდან და ქმნის ა იონური ბმა.
ეს ნაერთები წყალში არ იხსნება, გარდა ამონიუმის კარბონატისა ((NH)4)2კომპანია3) და ტუტე მეტალებით წარმოქმნილი კარბონატები (1 ოჯახის ელემენტები: Li, Na, K, Rb, Cs და Fr). თითქმის ყველა თეთრი მყარია, როგორც ნაჩვენებია ქვემოთ მოცემულ სურათზე:

კარბონატების ორი ყველაზე გავრცელებული და ყველაზე მნიშვნელოვანი ყოველდღიური მაგალითია ნატრიუმის კარბონატი (Na2კომპანია3) და კალციუმის კარბონატი (CaCO)3). პირველ შემთხვევაში, ნატრიუმი მიეკუთვნება 1 ოჯახს, რომელსაც აქვს ელექტრონი ვალენტურ გარსში და ცდილობს დაკარგოს ეს ელექტრონი, რომ გახდეს სტაბილური. რადგან კარბონატულ ანიონს ორი ელექტრონის მიღება სჭირდება, იგი უკავშირდება ნატრიუმის ორ ატომს:

სოდა ნაცარი უფრო ცნობილია, როგორც სოდა ან სოდა, რომელიც გამოიყენება საპნის, საღებავების, მედიკამენტების, ქაღალდების წარმოებაში და საცურაო აუზების წყლის სამკურნალოდ. მაგრამ მისი ძირითადი გამოყენებაა კალციუმის კარბონატთან და ქვიშასთან მინის წარმოებაში.
კალციუმი არის ოჯახი 2, რომელსაც აქვს ორი ელექტრონის დაკარგვის ტენდენცია. ამრიგად, კალციუმის ატომი უკავშირდება კარბონატულ რადიკალს:

კალციუმის კარბონატი იმყოფება კირქვაში და მარმარილოში. საათზე სტალაქტიტები და სტალაგმიტები მღვიმეებში არსებული ამ კარბონატისგან შედგება; ჭურვები, მარჯანი რიფები და კვერცხის ნაჭუჭებიც. როდესაც კედლებს, ხის ჩემოდნებს და სხვა ადგილებს ვთეთრებთ, ვიყენებთ კალციუმის ჰიდროქსიდს (Ca (OH)2), რომელიც დროთა განმავლობაში რეაგირებს ატმოსფერულ ნახშირორჟანგთან და ქმნის კალციუმის კარბონატს.

კარბონატები ძალზე გავრცელებულია დედამიწის ზედაპირზე, ისევე როგორც მინერალების შემთხვევაში. მის კრისტალურ ქსელს შეუძლია განალაგოს სივრცეში ორი გზით: ორთორჰომბიული (როგორც ეს ნაჩვენებია მინერალურ არაგონიტთან დაკავშირებით ზემოთ, კალციუმის კარბონატის ფორმულასთან ერთად) და რომბობერალური ან ტრიგონალური, ისევე როგორც კალციტი (სხვა მინერალი, რომელიც შედგება კალციუმის კარბონატისგან).
კარბონატები რეაგირებენ მჟავების თანდასწრებით, გამოყოფენ CO2, რომელიც ადვილად ჩანს შუშხუნა.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია

