შეიძლება მოხდეს, რომ იყოს იგივე ელემენტის მჟავები, და ამ ელემენტს აქვს იგივე დაჟანგვის ნომერი (NOX), მაგრამ განსხვავებაა ჰიდრატაციის ხარისხებში.
მაგალითად, ქვემოთ, ჩვენ გვაქვს სამი მჟავა, რომლებიც წარმოიქმნება ელემენტის ფოსფორის (P) მიერ:
ჰ3მტვერი4 ჰ4პ2ო7 HPO3
გაითვალისწინეთ, რომ სამივე მჟავაში ფოსფორის დაჟანგვის რაოდენობაა +5; განსხვავება არის ჰიდრატაციის ხარისხში.
ამის საფუძველზე, ეს მჟავები დიფერენცირდება ნომენკლატურაში პრეფიქსით ორთო, პირო და მეტა.
ყველაზე დატენიანებულ მჟავას ორტო ჰქვია. მოცემულ მაგალითში პირველი (H3მტვერი4) ეწოდება მჟავა ორთოფოსფორული, რადგან ის ყველაზე მეტად ჰიდრატირებულია სამიდან. ორთოს პრეფიქსი არის სახარჯო, ამიტომ უმეტესად ამ მჟავას უბრალოდ ეძახიან ფოსფორმჟავა.
პრეფიქსი პირო და მეტა გამოიყენება ორთოს მჟავით, როგორც საცნობარო წერტილი:
- პიროსი: ორთოს 2 მოლეკულა მინუს 1 H მოლეკულა2ო
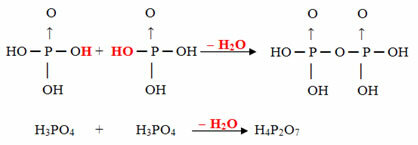
მაგალითი: H4პ2ო7 ეწოდება მჟავა პიროფოსფორული რადგან ის ორთოფოსფორმჟავას ორი მოლეკულის ტოლია (H3მტვერი4) მინუს ერთი წყლის მოლეკულა.
2. ჰ3მტვერი4 = თ6პ2ო8
ჰ6პ2ო8 - ჰ2O = H4პ2ო7
ეს პროცესი არის ინტერმოლეკულური დეჰიდრატაცია:
- მიზანი: ორთოს 1 მოლეკულა მინუს 1 H მოლეკულა2ო
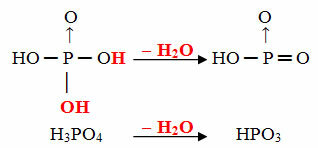
მაგალითი: HPO3 ეწოდება მჟავა მიზანიფოსფორული რადგან იგი ტოლია ორთოფოსფორული მჟავის მოლეკულის (H3მტვერი4) მინუს ერთი წყლის მოლეკულა.
ჰ3მტვერი4 - ჰ2O = HPO3
ეს პროცესი არის ინტრამოლეკულური დეჰიდრატაცია:
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/grau-hidratacao-dos-acidos.htm